Valeriaanzuur
Valeriaanzuur, ook wel pentaanzuur genoemd, is een organisch zuur met de formule C4H9COOH, waarbij de koolstofketen van 5 atomen onvertakt is. Valeriaanzuur is kleurloze vloeistof die onaangenaam ruikt.
Valeriaanzuur
| ||||
| Structuurformule en molecuulmodel | ||||
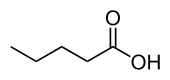 | ||||
Structuurformule van valeriaanzuur | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C5H1OO2 | |||
| IUPAC-naam | pentaanzuur | |||
| Molmassa | 102,13 g/mol | |||
| SMILES | CCCCC(=O)O | |||
| CAS-nummer | 109-52-4 | |||
| EG-nummer | 203-677-2 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H314 - H412 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P273 - P280 - P305+P351+P338 - P310 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos | |||
| Dichtheid | 0,9390 g/cm³ | |||
| Smeltpunt | −20 tot −18 °C | |||
| Kookpunt | 185 °C | |||
| Vlampunt | 86 °C | |||
| Zelfontbrandings- temperatuur | 440 °C | |||
| Viscositeit | 2,2 Pa·s | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Naast valeriaanzuur is ook isovaleriaanzuur bekend. Systematisch wordt die verbinding 3-methylbutaanzuur genoemd. De zouten en esters van valeriaanzuur worden valeraten genoemd.
Toepassingen
Het gebruik van valeriaanzuur beperkt zich tot de synthese van esters, die, in tegenstelling tot het zuur, aangenaam fruitig ruiken en daarom als geurstof gebruikt kunnen worden. Een voorbeeld is methylvaleraat, dat naar ananas geurt.
| Carbonzuren | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
This article is issued from
Wikipedia.
The text is licensed under Creative
Commons - Attribution - Sharealike.
Additional terms may apply for the media files.