Etheen
Etheen (ook bekend onder de oudere naam ethyleen) is een koolwaterstof met als brutoformule C2H4. Het is een vlak molecule met drie tweetallige rotatieassen, een inversiepunt en drie spiegelvlakken. Het behoort tot de puntgroep D2h. Het is de eenvoudigste koolwaterstof met een dubbele binding. Daarmee behoort het tot de stofklasse der alkenen.
Etheen
| |||||
| Structuurformule en molecuulmodel | |||||
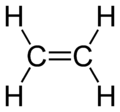 | |||||
Structuurformule van etheen | |||||
| Algemeen | |||||
| Molecuulformule (uitleg) | C2H4 | ||||
| IUPAC-naam | etheen | ||||
| Andere namen | ethyleen | ||||
| Molmassa | 28,05 g/mol | ||||
| SMILES | C=C | ||||
| CAS-nummer | 74-85-1 | ||||
| EG-nummer | 200-815-3 | ||||
| Beschrijving | Kleurloos en reukloos gas | ||||
| Vergelijkbaar met | ethyn, propeen, ethaan | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H220 - H336 | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P210 - P261 | ||||
| Opslag | Gasfles verwijderd houden van hitte, vonken of open vlammen; de temperatuur mag in geen geval boven 52°C uitkomen wegens het explosiegevaar; mengsels van aluminiumchloride en etheen warmen snel op en kunnen ontploffen bij 30-60 bar; reacties met chloorgas, ozon of stikstofoxiden zijn explosief | ||||
| VN-nummer | 1962 | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | gasvormig | ||||
| Kleur | kleurloos | ||||
| Dichtheid | 1,78 g/cm³ | ||||
| Smeltpunt | −169,15 °C | ||||
| Kookpunt | −103,71 °C | ||||
| Vlampunt | −100 °C | ||||
| Zelfontbrandings- temperatuur | 425 °C | ||||
| Thermodynamische eigenschappen | |||||
| ΔfH | 52,47 kJ/mol | ||||
| S | 219,32 J/mol·K | ||||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Etheen is een zeer belangrijke grondstof voor allerlei andere verbindingen, waaronder het polymeer polyetheen. Etheen is de meest geproduceerde petrochemische stof ter wereld; in 1996 bedroeg de totale productiecapaciteit 79,3 miljoen ton.
Productie
De productie van etheen vindt plaats door het stoomkraken van ethaan, LPG (propaan/butaan-mengsel) en nafta's. Dit zijn mengsels van koolwaterstoffen met een kookpunt tussen 30 °C en 200 °C afkomstig van de destillatie van aardolie, gasolie of zelfs hoogmoleculaire wassen. In een stoomkraker (steam cracker) worden deze koolwaterstoffen gemengd met stoom en gedurende korte tijd (0,1 tot 0,5 seconde) blootgesteld aan een zeer hoge temperatuur (tot 875 °C). De koolwaterstoffen breken daardoor op in kleinere moleculen, waarvan de voornaamste de onverzadigde koolwaterstoffen etheen, propeen, buteen en 1,3-butadieen zijn. Deze worden dan van elkaar gescheiden in een opeenvolging van destillatietorens en andere chemische bewerkingen.
Andere grondstoffen voor etheen zijn aardgas en raffinaderijgas (restgas van petroleumraffinaderijen).
Toepassingen
Etheen op zichzelf heeft weinig rechtstreekse toepassingen; het wordt vrijwel uitsluitend gebruikt als bouwsteen voor andere verbindingen. De meest belangrijke etheenverbruikende industriële processen zijn:
- polymerisatie tot LDPE (lage-dichtheid polyetheen) en LLDPE (lineair lage-dichtheid polyetheen)
- polymerisatie tot HDPE (hoge-dichtheid polyetheen)
- additie van dichloor met vorming van 1,2-dichloorethaan
- oxidatie tot etheenoxide (oxiraan)
- reactie met benzeen tot ethylbenzeen
- oxidatie tot aceetaldehyde
- hydratatie tot ethanol
- reactie met azijnzuur en zuurstofgas tot vinylacetaat
Andere processen zijn de productie van lineaire alcoholen, alkenen, chloorethaan en de copolymerisatie met propeen tot ethyleen-propyleen- (EP) en ethyleen-propyleen-dieen-rubber (EPDM).
Voorkomen in planten
Etheen is een hormoon in planten, waar het verschillende effecten heeft. Eén ervan is dat etheen wordt geproduceerd door sommige rijpende vruchten. Deze worden climacterische vruchten genoemd. Enkele voorbeelden van climacterische vruchten zijn appels, passievruchten, bananen, kaki's, avocados en tomaten. Niet-climacterische vruchten zullen slechts spoorhoeveelheden etheen aanmaken bij fruitrijping en exogeen toevoegen ervan zal de rijping niet doen toenemen.
Voor bloeminductie bij bromelia's wordt meestal gebruikgemaakt van ethyn of acetyleen,[1] maar ook etheen kan hiervoor gebruikt worden.
Etheen kan gebruikt worden voor het sneller laten rijpen van bananen (een mengsel van ca. 5% etheen en 95% stikstofgas wordt als banana gas verkocht). Doordat bananen van nature al veel etheen afscheiden, werden ze vroeger in fruitkoelhuizen gebruikt om het rijpingsproces van andere vruchten te versnellen. Sinds 1999 is bekend dat men etheen kan gebruiken voor de kiemremming bij uien en aardappelen. Snijbloemen verwelken onder invloed van etheen. Daarom mogen vruchten en bloemen nooit samen vervoerd worden. Om dit effect tegen te gaan wordt wel gebruikgemaakt van 1-methylcyclopropeen.
Etheen wordt ook vaak beschouwd als het stress-hormoon van planten. Wanneer deze bijvoorbeeld te maken krijgen met hoge temperatuur of hoge concentratie toxische stoffen, zal de etheenproductie aanzienlijk stijgen.
Functie
Hoewel snelle rijping economisch nadelig is, bestaat er voor planten die gevoelig zijn voor etheen een duidelijk voordeel: rijpende vruchten (zoals bananen) produceren etheen, waardoor vruchten in de buurt ook rijpen. De vruchten zullen dus in een grote hoeveelheid gelijktijdig rijp zijn. Zowel het aantrekken van dieren die voor de verspreiding nodig zijn als het feit dat de dieren niet alle vruchten zullen kunnen opeten, biedt een grotere kans op verspreiding van de vruchten en daarmee de soort plant.
Biosynthese
In hogere planten wordt etheen gesynthetiseerd op basis van het aminozuur methionine. Methionine wordt door ATP geactiveerd (Yang-cyclus) tot S-adenosyl-L-methionine (SAM). Vervolgens zal het ACC-synthase, een enzym, in het cytoplasma SAM omzetten tot 1-aminocyclopropaan-1-carbonzuur (ACC). Uiteindelijk kan ACC omgezet worden tot etheen of geconjugeerd worden tot onder andere malonyl-ACC (MACC). De omzetting van ACC tot etheen gebeurt onder invloed van het enzym ACC-oxidase in de vacuole of bij het plasmamembraan. Dit enzym heeft zuurstofgas nodig om te werken. Hierdoor zal etheensynthese niet doorgaan in een anaeroob milieu.
De omvorming van SAM tot ACC kan door auxines sterk bevorderd worden. Hierdoor worden de effecten van auxines op planten vaak beïnvloed door de hoeveelheid etheen.
Externe links

- (en) Gegevens van Etheen in de GESTIS-stoffendatabank van het Duitse Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA) (JavaScript vereist)
- MSDS van etheen[dode link]


