Asparaginezuur
Asparaginezuur (afgekort tot Asp of D) is een van de twintig natuurlijk voorkomende aminozuren die de bouwstenen zijn van eiwitten. De stof komt voor als kleurloze schilferige of naaldvormige kristallen, die slecht oplosbaar zijn in water.
Asparaginezuur
| ||||
| Structuurformule en molecuulmodel | ||||
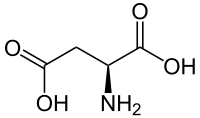 | ||||
Structuurformule van L-asparaginezuur | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C4H7NO4 | |||
| IUPAC-naam | (2S)-2-aminobutaandizuur | |||
| Andere namen | 2-aminobutaandizuur, aspartaamzuur | |||
| Molmassa | 133,10268 g/mol | |||
| SMILES | C([C@@H](C(=O)O)N)C(=O)O | |||
| InChI | 1/C4H7NO4/c5-2(4(8)9)1-3(6)7/h2H,1,5H2,(H,6,7)(H,8,9)/t2-/m0/s1/f/h6,8H | |||
| CAS-nummer | 56-84-8 | |||
| EG-nummer | 200-291-6 | |||
| PubChem | 5960 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H319 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P305+P351+P338 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,66 g/cm³ | |||
| Smeltpunt | 270-271 °C | |||
| Oplosbaarheid in water | 4 g/l | |||
| Slecht oplosbaar in | water | |||
| Thermodynamische eigenschappen | ||||
| ΔfH | −973,3 kJ/mol | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Zouten en esters van asparaginezuur worden aspartaten genoemd.
Asparaginezuur wordt gecodeerd door de codons GAU en GAC.
Ontdekking
Asparaginezuur werd in 1827 ontdekt door Plisson, doordat hij asparagine (dat een 20-tal jaar daarvoor al werd geïsoleerd uit asperges) behandelde met een base.
Synthese
Op industriële schaal wordt asparaginezuur bereid door additie van ammoniak aan de dubbele binding in fumaarzuur.[1] Daarbij worden bepaalde micro-organismen en het enzym L-aspartase ingezet. Het kan ook bereid worden door een transaminering van de ketonfunctie in oxaalazijnzuur.
Structuur
Het residu van asparaginezuur is een carboxylgroep die via een methyleengroep verbonden is met het centraal α-koolstofatoom. Daar aanwezigheid van de carboxylgroep bestaat mogelijkheid tot deprotonering, waarbij de carboxylaatgroep ontstaat. Bijgevolg wordt asparaginezuur geclassificeerd als een geladen aminozuur. Desondanks is het slecht oplosbaar in water.
Biochemische rol
Asparaginezuur is een van de niet-essentiële aminozuren bij zoogdieren, omdat het door een transaminering kan gevormd worden uit oxaalazijnzuur. Het kan ook gevormd worden in de ureumcyclus uit ornithine en citrulline. In planten en micro-organismen is aspartaat een belangrijke precursor van andere aminozuren, waaronder methionine, threonine, isoleucine en lysine. De omzetting van aspartaat naar deze aminozuren start met de reductie tot diens semi-aldehyde.[2]
Eigenschappen
Asparaginezuur is betrokken bij de vorming van glucose, de gluconeogenese en het is de precursor van aspartaat. Aspartaat is een excitatoire (stimulerende) neurotransmitter . Er wordt wel vermoed dat het functioneert om vermoeidheid tegen te gaan en dus een rol speelt bij het uithoudingsvermogen, maar daar is geen sterk bewijs voor.
De zuurconstanten van asparaginezuur zijn:[3]
- pKa1 (carboxylgroep) = 1,88
- pKaR (carboxylgroep in het residu) = 3,65
- pKa2 (aminegroep) = 9,60
Het iso-elektrisch punt ligt bij pH 2,77.[3]
Voorkomen
Aangezien asparaginezuur niet-essentieel is, hoeft het niet uitsluitend via de voeding te worden opgenomen. Asparaginezuur komt voor in: spruitjes, havervlokken, avocado, asperges, suikerriet en melasse van suikerbieten.
Zie ook
Externe links
- (en) MSDS van L-asparaginezuur
- (en) Gegevens van Asparaginezuur in de GESTIS-stoffendatabank van het Duitse Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA) (JavaScript vereist)
Bronnen, noten en/of referenties
|
| De 20 proteïnogene aminozuren |
|---|
|
Alanine (Ala) · Arginine (Arg) · Asparagine (Asn) · Asparaginezuur (Asp) · Cysteïne (Cys) · Glutamine (Gln) · Glutaminezuur (Glu) · Glycine (Gly) · Histidine (His) · Isoleucine (Ile) · Leucine (Leu) · Lysine (Lys) · Methionine (Met) · Fenylalanine (Phe) · Proline (Pro) · Serine (Ser) · Threonine (Thr) · Tryptofaan (Trp) · Tyrosine (Tyr) · Valine (Val) |
| Neurotransmitters |
|---|
|
acetylcholine (ACh) · adrenaline · anandamide · aspartaat (Asp) · β-lipoproteïne · bombesine · cholecystokinine (CCK) · corticotropine (ACTH) · dopamine (DA) · dynorfine · endorfine · enkefaline · γ-aminoboterzuur (GABA) · glutamaat (Glu) · glycine (Gly) · histamine · leumorfine · motiline · neurofysine I · neurofysine II · neurokinine A · neurokinine B · neuropeptide A · neuropeptide γ · neuropeptide Y · noradrenaline · peptide YY · serotonine (5-HT) · stikstofoxide (NO) · substantie P |
