Alanine
Alanine (afgekort tot Ala of A) is een van de twintig natuurlijk voorkomende aminozuren. In zuivere vorm is alanine een goed wateroplosbaar wit, kristallijn poeder.
Alanine
| ||||
| Structuurformule en molecuulmodel | ||||
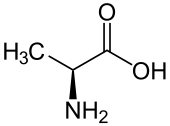 | ||||
Structuurformule van L-alanine | ||||
 | ||||
Molecuulmodel van L-alanine | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C3H7NO2 | |||
| IUPAC-naam | 2-aminopropaanzuur | |||
| Molmassa | 89,09318 g/mol | |||
| SMILES | NC(C)C(O)=O | |||
| InChI | 1S/C3H7NO2/c1-2(4)3(5)6/h2H,4H2,1H3,(H,5,6)/t2-/m0/s1 | |||
| CAS-nummer | 56-41-7 | |||
| EG-nummer | 200-273-8 | |||
| PubChem | 5950 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit | |||
| Dichtheid | 1,401 g/cm³ | |||
| Smeltpunt | 314,5 °C | |||
| Oplosbaarheid in water | 166,5 g/l | |||
| Goed oplosbaar in | water | |||
| Thermodynamische eigenschappen | ||||
| ΔfH | −465,9 kJ/mol | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Alanine wordt gecodeerd door de codons GCU, GCC, GCA en GCG.
Synthese
Biosynthese
De belangrijkste biochemische synthese van alanine in het lichaam verloopt via een reductieve aminering van pyrodruivenzuur. Omdat transamineringen in de regel reversibel zijn, kan alanine zeer gemakkelijk gemaakt worden. Deze syntheseroute is gekoppeld aan andere belangrijke biochemische processen, zoals de glycolyse, de gluconeogenese en de citroenzuurcyclus. Daarnaast kan alanine uit andere vertakte apolaire aminozuren, zoals valine, leucine en isoleucine gemaakt worden
Chemische synthese
L-Alanine werd in 1850 door Adolph Strecker gesynthetiseerd en benoemd. Hij koos deze naam als afgeleide van de benaming 'aldehyde', aangezien hij het aminozuur uit een aldehyde via de naar hem genoemde Strecker-aminozuursyntheseroute synthetiseerde. Het aminozuur werd in 1888 door T. Weyl als proteïnebestanddeel van zijdefibroïne gekarakteriseerd en daaruit geïsoleerd. Het zijdefibroïne bevat circa 29,7% L-alanine. Een racemisch mengsel van D- en L-alanine kan bereid worden door de Strecker-aminozuursynthese van aceetaldehyde met ammoniumchloride, in aanwezigheid van natriumcyanide:
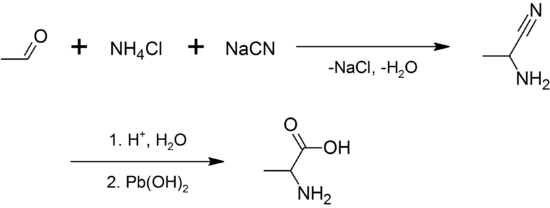 Synthese van alanine
Synthese van alanine
Een alternatieve methode is de ammonolyse van 2-broompropaanzuur:
 Synthese van alanine
Synthese van alanine
Structuur
Alanine is, na glycine, het meest eenvoudig aminozuur. De restgroep is een methylgroep en daarom wordt alanine geclassificeerd als een apolair aminozuur. Door de aanwezigheid van de polaire amine- en carbonzuurgroepen is het desondanks toch goed wateroplosbaar.
Voorkomen en eigenschappen
Goede bronnen van alanine zijn vlees, kip, vis en eieren. Ook sommige eiwitrijke planten zoals avocado zijn rijk aan alanine.
Het iso-elektrisch punt van alanine ligt bij pH 6,00.[1] De respectievelijk zuurconstanten zijn:[1]
- pKa1 (carboxylgroep) = 2,34
- pKa2 (aminegroep) = 9,69
Dierproeven hebben voor alanine een cholesterolverlagende werking aangetoond. Bij onderzoek bij mensen met CVS (chronischevermoeidheidssyndroom) werden verhoogde alanine waarden aangetoond en lage voor tyrosine en fenylalanine.
Bij eukaryoten is het aanwezige alanine linksdraaiend, dus L-alanine. Bij bacteriën komt D-alanine in de celwand voor. Penicilline doodt bacteriën doordat het op D-alanine aangrijpt. Daardoor hebben niet-bacteriën dus geen last van penicilline.
Glucose-alaninecyclus
Bij anaerobe glycolyse wordt door de spieren alanine uitgescheiden. Deze hoeveelheid blijkt echter veel groter te zijn dan verklaard kan worden uit de afbraak van spiereiwitten. In de spier worden aminogroepen van aminozuren overgedragen op pyruvaat via een transaminering. Hierdoor kan stikstof, dat vrijkomt bij de afbraak van spiereiwitten, op een veilige manier worden weggewerkt. De metabole last van de spier wordt dus als het ware op de lever geschoven. In de lever wordt alanine weer omgezet tot glucose en wordt de vrijkomende stikstof afgevoerd onder de vorm van ureum.[2]
Externe link
- (en) Gegevens van Alanine in de GESTIS-stoffendatabank van het Duitse Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA) (JavaScript vereist)
Bronnen, noten en/of referenties
|
| De 20 proteïnogene aminozuren |
|---|
|
Alanine (Ala) · Arginine (Arg) · Asparagine (Asn) · Asparaginezuur (Asp) · Cysteïne (Cys) · Glutamine (Gln) · Glutaminezuur (Glu) · Glycine (Gly) · Histidine (His) · Isoleucine (Ile) · Leucine (Leu) · Lysine (Lys) · Methionine (Met) · Fenylalanine (Phe) · Proline (Pro) · Serine (Ser) · Threonine (Thr) · Tryptofaan (Trp) · Tyrosine (Tyr) · Valine (Val) |