Aldehyde
Een aldehyde kan worden gemaakt door een primaire alcohol selectief te oxideren.
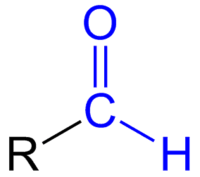
Algemene structuurformule van een aldehyde.
Een aldehyde (ook wel alkanal) is:
- een functionele groep, bestaande uit een carbonylgroep waaraan een waterstofatoom is gebonden.
- een organische chemische verbinding met zo'n groep.
Het eenvoudigste aldehyde is formaldehyde (H2C=O), dat in de vorm van een verdunde oplossing (formaline) als ontsmettings- en conserveringsmiddel wordt gebruikt (sterk water).
Andere aldehyden zijn onder andere
- Aceetaldehyde (ethanal, CH3-CHO)
- Propanal
- Butanal
- Isobutyraldehyde (isobutanal)
De naamgeving van de aldehyden met 3 of meer koolstofatomen wordt als volgt gedefinieerd: naam alkaan (alkeen, alkyn) + 'al'. Voorbeeld:
- propaan → propanal
- propeen → propenal
- butaan → butanal
- but-2-een → but-2-en-1-al
- but-2-yn → but-2-yn-1-al
Reacties
- Aldehyden reageren met waterstof via een additiereactie tot primaire alcoholen.
- Aldehyden kunnen met zuurstof geoxideerd worden tot carbonzuren.
- Aldehyden kunnen aangetoond worden met Haines reagens, fehlingsreagens, Benedicts reagens (alle op basis van Cu2+ → Cu+) en Tollens' reagens (op basis van Ag+ → Ago). In deze reacties ontstaat een carbonzuur met hetzelfde koolstofskelet als het aldehyde. Is niet zozeer de detectie van het aldehyde als de productie van het carbonzuur het doel van de reactie, dan wordt dichromaat-zwavelzuur als oxidator gebruikt.
Synthese
De synthese van aldehyden kan op verschillende manieren gerealiseerd worden.
- De directe synthese van aldehyden uit hun overeenkomstige alcoholen lijkt een eenvoudige partiële oxidatie, maar in de praktijk blijkt het lastig op deze wijze de aldehyden te bereiden. Vaak oxideert het aldehyde makkelijker dan het alcohol en is het carbonzuur het enige isoleerbare reactieproduct.
This article is issued from
Wikipedia.
The text is licensed under Creative
Commons - Attribution - Sharealike.
Additional terms may apply for the media files.