| Basiskennis chemie |
|
Chemie en Stoffen
Chemisch Rekenen
Naamgeving zouten
Hoeveel?
|
Atomen rangschikken
Orde in de chaos


.svg.png)
Was het idee van atomen en elementen rond 1800 in de wetenschap geaccepteerd, hoeveel elementen er waren was toen nog lang niet duidelijk. In de eerste helft van de 19e eeuw was de jacht op elementen open. In een hoog tempo werden steeds weer nieuwe elementen gevonden. Sommige leken op elkaar, zoals chloor, broom en jood, of de groep lithium, natrium, kalium. Ook koper, zilver en goud werden als groep herkend. Een algemeen overzicht ontbrak nog omdat niet duidelijk was hoeveel elementen er nu precies waren: de in Kern en elektronen genoemde lading van de kern, en het feit dat elk element zijn eigen kernlading heeft, werden pas aan het eind van de 19e eeuw bekend.
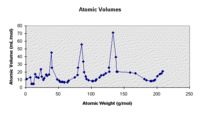
Los van elkaar bouwden Dmitri Mendelejev en Julius Lothar Meyer aan een totaaloverzicht van de elementen. Meyer bepaalde voor alle bekende elementen het volume van 1 mol van de stof. Als hij de resultaten uitzette tegen de molaire massa van het element, kreeg hij de grafiek zoals die hiernaast staat weergegeven. Omdat 1 mol stof steeds evenveel atomen bevat, zijn de relatieve verschillen en verhoudingen voor 1 mol of 1 atoom precies gelijk.
Mendelejev keek niet naar slechts één eigenschap maar naar zoveel mogelijk eigenschappen van de elementen die hij kende. Ook hij zette de elementen op volgorde van massa. Hij ging echter een stap verder.
Na zink ontbraken er, wat eigenschappen betreft twee elementen. Volgens Mendelejev waren die twee gewoon nog niet ontdekt!. Op grond van de eigenschappen van silicium en tin durfde hij de eigenschappen van het ontbrekende element, door hem eka-silicium genoemd en nu bekend als germanium, te voorspellen. Toen het element een aantal jaren later gevonden werd, bleken de eigenschappen, verbindingen en vindplaats opmerkelijk goed overeen te stemmen met de voorspellingen van Mendelejev.
Vergelijking tussen Mendelev's voorspelling in 1871 en de eigenschappen van gallium en germaninium Eigenschap Gallium[1] Germanium[2] Voorspelling Gemeten Voorspelling Gemeten Atoomgewicht ~68 69.723 72.64 72.59 Dichtheid (g/cm3) 5.9 5.904 5.5 5.35 Smeltpunt (°C) laag 29.767 hoog 947 Kleur grijs grijs oxide type Vuurvast dioxide vurvast dioxide Formule van het oxide Dichtheid van het oxide (g/cm3) 5.5 5.88 4.7 4.7 Type van het hydroxide amfoteer amfoteer Type oxide zwak basisch zwak basisch Formule van het chloride Kookpunt van het chloride (°C) < 100 86 () Dichtheid van het chloride (g/cm3) 1.9 1.9
Omdat Mendelejev nog niets wist over de kernlading of de elektronen had hij ook geen last van het feit dar de edelgassen nog niet bekend waren in zijn tijd. Ook op sommige plaatsen waar de molaire massa van een volgend element net iets lager uitvalt, was voor hem geen probleem omdat een van de twee elementen nog niet gevonden was.
Omdat kenmerkende eigenschappen zich periodiek in de lijst herhalen, wordt de tabel die door Mendelejev ontworpen werd aangeduid met de naam: Periodiek Systeem der Elementen, of kortweg periodiek systeem. Vandaag de dag kunnen we deze periodiciteit verklaren uit de opbouw van de elektronenwolk. Omdat de meer naar buiten gelegen schillen meer elektronen kunnen bevatten (zie de paragraaf over elektronenschillen
Het periodiek systeem
Het blijkt dat als de verschillende atoomsoorten worden gerangschikt in een tabel op volgorde van hun atoomnummer van linksboven naar rechtsonder met rijen van bepaalde lengte dan vormen de atoomsoorten in de kolommen families met gelijkaardige eigenschappen. De tabel heet het periodiek systeem der elementen (PSE).
Het totaal van de elementen bedraagt: 2 + 8 + 8 + 18 + 18 + 32 + 32 = 118.
Huidige systeem
| Het periodiek systeem der elementen | ||||||||||||||||||
| 1 Ia |
18 0 | |||||||||||||||||
| 1 | 1 H |
2 IIa |
13 IIIa |
14 IVa |
15 Va |
16 VIa |
17 VIIa |
2 He | ||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | ||||||||||
| 3 | 11 Na |
12 Mg |
3 IIIb |
4 IVb |
5 Vb |
6 VIb |
7 VIIb |
8 VIIIb |
9 VIIIb |
10 VIIIb |
11 Ib |
12 IIb |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar |
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr |
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
(43) Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe |
| 6 | 55 Cs |
56 Ba |
* |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn |
| 7 | 87 Fr |
88 Ra |
** |
(104) Rf |
(105) Db |
(106) Sg |
(107) Bh |
(108) Hs |
(109) Mt |
(110) Ds |
(111) Rg |
(112) Cn |
(113) Nh |
(114) Fl |
(115) Mc |
(116) Lv |
(117) Ts |
(118) Og |
| *Lanthaniden | 57 La |
58 Ce |
59 Pr |
60 Nd |
(61) Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu | |||
| **Actiniden | 89 Ac |
90 Th |
91 Pa |
92 U |
(93) Np |
(94) Pu |
(95) Am |
(96) Cm |
(97) Bk |
(98) Cf |
(99) Es |
(100) Fm |
(101) Md |
(102) No |
(103) Lr | |||
De kolommen van het PSE heten groepen, genummerd van 1 tot en met 18, en de rijen, heten periodes, genummerd van 1 tot en met 7. De groepen 1,2,13,..,18 heten hoofdgroepen en de groepen 3,..,12 overgangsmetalen.
Periode 1 heeft twee groepen, H waterstof en He Helium. Periode 2 en 3 hebben elk 8 groepen. In periode 4 tot en met 7 worden 10 groepen toegevoegd. In periode 6 en 7 bestaat groep 3 uit 15 elementen. respectievelijk de lanthaniden en actiniden genaamd.
Speciale namen
Groepen worden, met name die met de overgangsmetalen, benoemd door het bovenste element van de groep. Daarnaast worden ook onderstaande benamingen vaak gebruikt:
- Alkalimetalen
De elementen in groep 1, behalve waterstof. Als metaal reageren deze elementen allemaal heftig tot zeer heftig met water onder vorming van een loog. - Aardalkalimetalen
Deze elementen staan in groep 2. Ze reageren ook met water, maar minder heftig dan hun buren in groep 1 in dezelfde periode. - Halogenen
De naam van deze groep betekent "zoutvormers". De bekendste vertegenwoordiger is chloor, dat als chloride deel uitmaakt van keukenzout. - Edelgassen
De laatst ontdekte groep in het periodiek systeem. De atomen van deze elementen hebben allemaal een volle of voorlopig volle valentieschil. Hierdoor reageren ze allemaal niet of met grote moeite met andere elementen.
Het Periodiek systeem in 1869
In onderstaande tabel zijn de molaire massa's vermeld met de nauwkeurigheid zoals die in 1869 bekend was, op één decimaal. Hoewel de rode draad wel de oplopende molaire massa is, geven de rode vakjes aan waar Medelejev de moed had te volgorde om te draaien om de eigenschappen van de elementen op de juiste wijze te rangschikken.
Van de groen aangegeven elementen zijn door Mendelejev goede voorspellingen van de eigenschappen gedaan.
| De elementen die 1869 bekend waren in het periodiek systeem. | ||||||||||||||||||
| 1 Ia |
18 0 | |||||||||||||||||
| 1 | H 1.0 |
2 IIa |
13 IIIa |
14 IVa |
15 Va |
16 VIa |
17 VIIa |
|||||||||||
| 2 | Li 6.9 |
Be 9.0 |
B 10.8 |
C 12.0 |
N 14.0 |
O 16.0 |
||||||||||||
| 3 | Na 23.0 |
Mg 24.3 |
3 IIIb |
4 IVb |
5 Vb |
6 VIb |
7 VIIb |
8 VIIIb |
9 VIIIb |
10 VIIIb |
11 Ib |
12 IIb |
Al 27.0 |
Si 28.1 |
P 31.0 |
S 32.1 |
Cl 35.5 |
|
| 4 | K 39.1 |
Ca 40.1 |
Ti 45.0 |
V 50.9 |
Cr 52.0 |
Mn 54.9 |
Fe 55.9 |
Co 58.9 |
Ni 58.7 |
Cu 63.6 |
Zn 65.4 |
As 74.9 |
Se 79.0 |
Br 79.9 |
||||
| 5 | Rb 85.5 |
Sr 87.6 |
Y 88.9 |
Zr 91.2 |
Nb 92.9 |
Mo 95.9 |
Ru 101.1 |
Rh 102.9 |
Pd 106.4 |
Ag 107.9 |
Cd 112.4 |
In 114.8 |
Sn 118.7 |
Sb 121.8 |
Te 127.6 |
I 126.9 |
||
| 6 | Cs 132.9 |
Ba 137.3 |
* |
Ta 180.9 |
W 183.9 |
Os 190.2 |
Ir 192.2 |
Pt 195.1 |
Au 197.0 |
Hg 200.6 |
Tl 204.4 |
Pb 207.2 |
Bi 209.0 |
|||||
| 7 | ** |
|||||||||||||||||
| *Lanthaniden | La 138.9 |
Ce 140.1 |
Sm 150.4 |
Tb 159.9 |
Er 167.3 |
|||||||||||||
| **Actiniden | Th 232.0 |
U 238.0 |
||||||||||||||||