| Basiskennis chemie |
|
Chemie en Stoffen
Chemisch Rekenen
Naamgeving zouten
Hoeveel?
|
Naamgeving van zouten
|
Zouten bestaan uit elektrisch positief en negatief geladen ionen. De naamgeving van zouten is in principe recht toe recht aan: eerst het positieve ion, dan het negatieve ion. Verder is een zout als geheel elektrisch neutraal, dus de formule ervan moet zo zijn dat de totale positieve lading gelijk is aan de totale negatieve lading. Vaak zal het nodig zijn van een of beide ionen meer dan een ion in de formule op te nemen. |
Voorbeelden
Natriumchloride
|
Natriumchloride
|
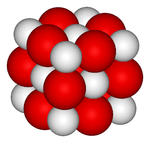
Calciumoxide
|
Calciumoxide
|
IJzer(III)fosfaat
|
IJzer(III)fosfaat Stukjes ijzer(III)fosfaat
|
|
De voorgaande voorbeelden gingen steeds over stoffen, waarbij de lading van de positieve en de negatieve ionen gelijk is. In onderstaande voorbeelden zijn de ladingen van de ionen niet gelijk. Dit zien we vooral terug in de formules van de zouten. |
Calciumchloride
|
Calciumchloride Calcium met twee chloride-ionen
|
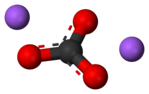
Natriumcarbonaat
|
Natriumcarbonaat Twee natrium-ionen met een carbonaat-ion
|
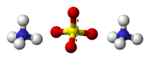
Ammoniumsulfaat
|
Ammoniumsulfaat Twee ammonium-ionen met een sulfaat-ion
|
Chroom(III)sulfaat
|
Chroom(III)sulfaat Twee chroom-ionen met drie sulfaat-ionen.
|

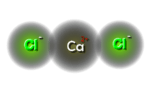
sulfaat.png)