CS-gas
CS-gas, de triviale naam voor ortho-chloorbenzylideenmalononitril, is een toxische en irriterende organische chloorverbinding, met als brutoformule C10H5ClN2. De stof komt voor als een wit kristallijn poeder met kenmerkende geur. CS-gas is zeer slecht oplosbaar in water, maar zeer goed in aceton en DMSO.
CS-gas
| |||||
| Structuurformule en molecuulmodel | |||||
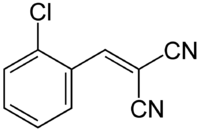 | |||||
Structuurformule van CS-gas | |||||
 | |||||
Molecuulmodel van CS-gas | |||||
| Algemeen | |||||
| Molecuulformule (uitleg) | C10H5ClN2 | ||||
| IUPAC-naam | 2-(chloorfenyl)methyleennitril | ||||
| Andere namen | o-(chloorfenyl)methyleenmalonnitril, (2-chloorfenyl)methyleenpropaandinitril, β-,β-dicyaan-o-chloorstyreen, CS, NCI-C55118, USAF KF-11, 2-chloor-BMN | ||||
| Molmassa | 188,6131 g/mol | ||||
| SMILES | C1(=CC=CC=C1C=C(C#C)C#C)Cl | ||||
| InChI | 1/C10H5ClN2/c11-10-4-2-1-3-9(10)5-8(6-12)7-13/h1-5H | ||||
| CAS-nummer | 2698-41-1 | ||||
| Beschrijving | Wit kristallijn poeder met kenmerkende geur | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H301 - H311 - H315 - H319 - H331 | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P264 - P270 - P301+P310 - P321 - P330 | ||||
| Opslag | Gescheiden van voeding en voedingsmiddelen. Goed gesloten en in een goed verluchte ruimte bewaren. | ||||
| VN-nummer | 3276 | ||||
| ADR-klasse | Gevarenklasse 6.1 | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | vast | ||||
| Kleur | wit | ||||
| Dichtheid | 1,04 g/cm³ | ||||
| Smeltpunt | 93-96 °C | ||||
| Kookpunt | 310-315 °C | ||||
| Dampdruk | 0,0045 Pa | ||||
| Oplosbaarheid in water | (bij 20°C) 1-5 g/l | ||||
| Goed oplosbaar in | aceton, dimethylsulfoxide | ||||
| Slecht oplosbaar in | water | ||||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
De afkorting CS verwijst naar de achternamen van de ontdekkers van deze stof, Ben B. Corson en Roger W. Stoughton.[1] Ze ontdekten CS-gas aan het Middlebury College in 1928.
Ondanks het feit dat het als gas wordt bestempeld, is de stof wel degelijk een vaste stof. De voornaamste toepassing van CS-gas is als traangas. Het werd in de jaren '50 en '60 van de 20ste eeuw heimelijk ontwikkeld in Porton Down, een militair domein in Wiltshire (Engeland). Aanvankelijk werd de werking van de stof getest op proefdieren, later op vrijwilligers uit het British Army.
Synthese
CS-gas wordt bereid uit een reactie van 2-chloorbenzaldehyde en propaandinitril, aan de hand van een Knoevenagel-condensatie:
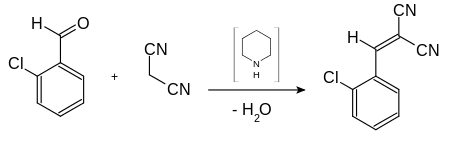 Bereiding van CS-gas
Bereiding van CS-gas
Deze reactie wordt gekatalyseerd aan de hand van een zwakke base, zoals piperidine of pyridine. De methode voor de bereiding is sedert de ontdekking in 1928 nog niet gewijzigd.[2] Er zijn andere methoden gesuggereerd om de opbrengst en het rendement te verhogen: gebruik van andere basen als katalysator, het weglaten van oplosmiddelen en technieken die gebruikmaken van microgolven.[3]
Toxicologie en veiligheid
De fysische eigenschappen van de stof werden al beschreven bij de ontdekking: Certain of these dinitriles have the effect of sneeze and tear gases. They are harmless when wet but to handle the dry powder is disastrous.[4]
CS-gas reageert hevig met sterke basen en sterke zuren, met vorming van ammoniak. De stof ontleedt bij verbranding, met vorming van giftige dampen, waaronder waterstofchloride, waterstofcyanide en stikstofoxiden. Ze reageert hevig met sterk oxiderende stoffen, waardoor kans op brand en ontploffing ontstaat.
CS-gas is sterk irriterend en kan ernstige schade aan de ogen en de longen veroorzaken. Bij inhalatie veroorzaakt dit meestal ongewenste effecten, zoals hoesten, duizeligheid, hoofdpijn, moeizame en pijnlijke ademhaling, misselijkheid, keelpijn en braken. Bij contact met de huid kan er een branderig gevoel ontstaan en kan er blaarvorming optreden. Aangezien CS-gas een lacrimator is, veroorzaakt de stof tranende ogen.
De stof is op zich vrij toxisch en kan schade berokkenen aan het hart en de lever.[5] Bovendien wordt gesuggereerd dat contact met CS-gas zou kunnen leiden tot miskramen, aangezien de stof clastogene effecten (abnormale wijzigingen in de chromosoomstructuur) heeft op cellen van zoogdieren.
CS-gas is evenwel niet dodelijk, maar kan ernstige en blijvende letsels veroorzaken indien men onvoldoende beschermd is.
Gebruik als aerosol
CS-gas komt voor als vaste stof, maar wordt voornamelijk gebruikt als aerosol. Er zijn verschillende technieken om van CS-poeder een aerosol te maken:
- Gebruikmaken van gesmolten CS-poeder
- CS-poeder oplossen in een organisch oplosmiddel
- Gebruikmaken van CS2, een micro-verpulverde vorm van CS-poeder, die behandeld is met silicium
CS-gas in het nieuws
- Op 6 mei 2009 werd bij een 23-jarige man uit Emmeloord CS-gas aangetroffen. Hij werd gearresteerd, omdat het volgens de Nederlandse Wet Wapens en Munitie verboden is om CS-gas te bezitten zonder vergunning.[6]
- In Bil'in, een dorp ten westen van de Palestijnse stad Ramallah, raakten in augustus 2009 Palestijnse opstandelingen slaags met het Israëlische leger. Dat zou CS-gas gebruikt hebben om de opstanden in te tomen.[7]
- Op 8 december 2018 verloor een protestant tijdens de gele hesjes-demonstraties in Parijs zijn hand toen hij een granaat met CS-gas probeerde terug te gooien naar de oproerpolitie.
Externe links

- (en) 2-Chlorobenzalmalononitrile op NIST (National Institute of Standards and Technology)
Bronnen, noten en/of referenties
|
| Chemische wapens | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
|


