4-nitroaniline
4-nitroaniline is een aromatische verbinding met als brutoformule C6H6N2O2. De stof komt voor als gele of bruine kristallen of als poeder. Het bestaat uit een benzeenring (vandaar het aromatisch karakter van de molecule), waaraan een NH2-groep en een NO2-groep zijn vastgehecht.
4-nitroaniline
| ||||
| Structuurformule en molecuulmodel | ||||
 | ||||
Structuurformule van 4-nitroaniline | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C6H6N2O2 | |||
| IUPAC-naam | 4-nitroaniline | |||
| Andere namen | para-nitroaniline, p-nitroaniline, 4-nitrobenzeenamine, 1-amino-4-nitrobenzeen | |||
| Molmassa | 138,12404 g/mol | |||
| CAS-nummer | 100-01-6 | |||
| EG-nummer | 202-810-1 | |||
| Beschrijving | Gele of bruine kristallen of poeder | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H301 - H311 - H331 - H373 - H412 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P261 - P273 - P280 - P301+P310 - P311 | |||
| Carcinogeen | mogelijk (IARC-klasse 3) | |||
| Opslag | Gescheiden van sterke zuren, sterk oxiderende stoffen, brandbare en reducerende stoffen, voeding en voedingsmiddelen. Droog bewaren. | |||
| EG-Index-nummer | 612-012-00-9 | |||
| VN-nummer | 1661 | |||
| LD50 (ratten) | (oraal) 450 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | geel-bruin | |||
| Dichtheid | 1,4 g/cm³ | |||
| Smeltpunt | 146-149 °C | |||
| Kookpunt | 332 °C | |||
| Vlampunt | 199 °C | |||
| Dampdruk | 0,2 Pa | |||
| Oplosbaarheid in water | (bij 18,5°C) 0,8 g/l | |||
| Goed oplosbaar in | ethanol, di-ethylether, chloroform | |||
| Slecht oplosbaar in | water | |||
| Evenwichtsconstante(n) | pKa = 1,00 | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
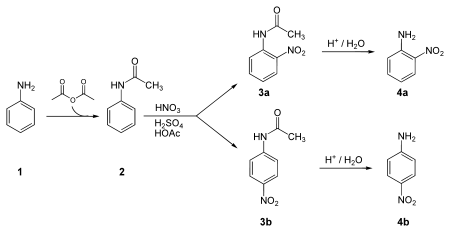
4-nitroaniline wordt gesynthetiseerd uit aniline (1). Eerst wordt met behulp van azijnzuuranhydride een acetaatgroep als beschermende groep aan aniline gekoppeld waardoor acetanilide (2) ontstaat. De NH2-groep van aniline moet beschermd worden, omdat anders in de volgende stap naast nitrering ook oxidatie zou optreden. Een tweede voordeel wordt gevormd door de grootte van de beschermende groep: de reactie op de 2-plaats wordt lastiger door sterische hindering.
Hierna volgt de aromatische nitrering met salpeterzuur, zwavelzuur en azijnzuur tot 2-nitroacetanilide (3a) en 4-nitroacetanilide (3b). Ten slotte wordt de beschermende acetaatgroep onder invloed van een zure katalysator afgesplitst, zodat men 4-nitroaniline (4b) en een kleine hoeveelheid 2-nitroaniline (4a) bekomt, die daarna wordt verwijderd.[1]
Industrieel wordt 4-nitroaniline ook bereid door p-chloornitrobenzeen te reageren met ammoniak.[2]
Toepassingen
4-nitroaniline wordt gebruikt als tussenstof in de synthese van kleurstoffen, antioxidanten, geneesmiddelen en benzine. Ze wordt ook aangewend in rubberinhibitoren, geneesmiddelen voor pluimvee en als beschermer tegen corrosie.
Toxicologie en veiligheid
De stof vormt bij verbranding giftige dampen van stikstofoxiden. Ze reageert met sterke zuren, sterk oxiderende stoffen en sterk reducerende stoffen. 4-nitroaniline reageert met organische materialen in aanwezigheid van vocht, waardoor kans op brand ontstaat. De stof is niet corrosief, maar erg toxisch.
De stof is matig irriterend voor de ogen en luchtwegen, maar erg schadelijk wanneer het in contact met de huid komt. 4-nitroaniline kan effecten hebben op het bloed, met als gevolg de vorming van methemoglobine. De effecten kunnen met vertraging optreden. De substantie is niet onder te brengen voor wat betreft de carcinogeniciteit voor de mens en behoort dus tot IARC-klasse 3.
Zie ook
Externe links
| Bronnen, noten en/of referenties |