Kaliumoxide
Kaliumoxide is het oxide van kalium, met als brutoformule K2O. De stof komt voor als een hygroscopische, kleurloze tot witte vaste stof.
Kaliumoxide
| ||||
| Structuurformule en molecuulmodel | ||||
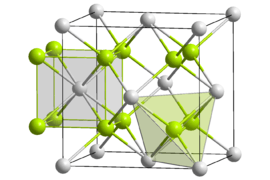 | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | K2O | |||
| IUPAC-naam | kaliumoxide | |||
| Molmassa | 94,196 g/mol | |||
| CAS-nummer | 12136-45-7 | |||
| PubChem | 25520 | |||
| Beschrijving | Zeer hygroscopische witte vaste stof | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| Hygroscopisch? | ja | |||
| Opslag | Bewaren in een van de lucht afgesloten container. | |||
| EG-Index-nummer | 235-227-6 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | witgrijs | |||
| Dichtheid | 2,35 g/cm³ | |||
| Smeltpunt | > 490 °C | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Kaliumoxide kan bereid worden door oxidatie van kalium met zuurstofgas:
De verbinding kan ook bereid worden door reductie van kaliumperoxide of kaliumnitraat met metallisch kalium:
Eigenschappen en reacties
De stof reageert hevig met water tot kaliumhydroxide:
Om die reden is kaliumoxide niet stabiel aan de lucht en ook corrosief voor de huid en ogen.
Toepassingen
De stof wordt wel in plaats van lood(II)oxide gebruikt als toevoeging in kristalglas.
Externe links
This article is issued from
Wikipedia.
The text is licensed under Creative
Commons - Attribution - Sharealike.
Additional terms may apply for the media files.