Hydrochinon
Hydrochinon of p-hydrochinon (IUPAC-naam: benzeen-1,4-diol) is een aromatische verbinding, bestaande uit een benzeenring waaraan twee hydroxylgroepen verbonden zijn. Het is een van de drie dihydroxybenzeen-isomeren; de andere twee zijn resorcinol (1,3-dihydroxybenzeen) en catechol (1,2-dihydroxybenzeen). De zuivere stof komt voor als kleurloze tot witte naaldvormige kristallen.
Hydrochinon
| ||||||
| Structuurformule en molecuulmodel | ||||||
 | ||||||
Structuurformule van hydrochinon | ||||||
 | ||||||
Hydrochinon-kristallen | ||||||
| Algemeen | ||||||
| Molecuulformule (uitleg) | C6H6O2 | |||||
| IUPAC-naam | bezeen-1,4-diol | |||||
| Andere namen | hydrochinon, 1,4-dihydroxybenzeen, 1,4-benzeendiol, β-chinol, p-hydroxyfenol | |||||
| Molmassa | 110,1 g/mol | |||||
| SMILES | OC1=CC=C(O)C=C1 | |||||
| CAS-nummer | 123-31-9 | |||||
| EG-nummer | 204-617-8 | |||||
| Beschrijving | Witte tot kleurloze kristallen | |||||
| Vergelijkbaar met | catechol, resorcinol | |||||
| Waarschuwingen en veiligheidsmaatregelen | ||||||
| ||||||
| H-zinnen | H302 - H317 - H318 - H341 - H351 - H400 | |||||
| EUH-zinnen | geen | |||||
| P-zinnen | P273 - P280 - P305+P351+P338 | |||||
| Carcinogeen | mogelijk | |||||
| EG-Index-nummer | 604-005-00-4 | |||||
| VN-nummer | 2662 | |||||
| ADR-klasse | Gevarenklasse 6.1 | |||||
| LD50 (ratten) | 320 mg/kg | |||||
| Fysische eigenschappen | ||||||
| Aggregatietoestand | vast | |||||
| Kleur | wit | |||||
| Dichtheid | 1,3 g/cm³ | |||||
| Smeltpunt | 172 °C | |||||
| Kookpunt | 287 °C | |||||
| Vlampunt | 165 °C | |||||
| Zelfontbrandings- temperatuur | 515 °C | |||||
| Oplosbaarheid in water | 70 g/l | |||||
| Goed oplosbaar in | water | |||||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||||
| ||||||
Synthese
Er bestaan verscheidene reactiewegen om hydrochinon te bereiden:
- de reductie van 1,4-benzochinon tot hydrochinon
- de oxidatie van p-di-isopropylbenzeen tot het dihydroperoxide, gevolgd door de ontleding daarvan (met vorming van aceton)
- de hydroxylering van fenol met waterstofperoxide in aanwezigheid van een zure katalysator
De productie van hydrochinon uit fenol langs biochemische weg is beschreven door Japanse onderzoekers van Mitsubishi Gas Chemical Co. in 1990.[1] Een specifieke bacterie (Mycobacterium sp. B-394) neemt hierbij de rol van biokatalysator over.
Eigenschappen
Hydrochinon is een milde reductor en kan via een reversibel proces geoxideerd worden tot 1,4-benzochinon:
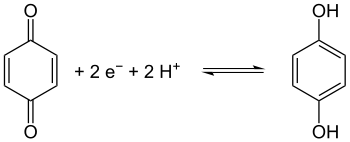 Redoxreactie tussen hydrochinon en 1,4-benzochinon
Redoxreactie tussen hydrochinon en 1,4-benzochinon
De hydroxylgroepen zijn zwak zuur: hierbij kunnen één of twee protonen (H+) afgestaan worden, waarbij respectievelijk het mono- en difenolaatanion gevormd worden.
Toepassingen
Wegens het reducerende karakter werd hydrochinon veel gebruikt in de (niet-digitale) fotografie als bestanddeel, meestal gecombineerd met metol, van ontwikkelaar-oplossingen (voor zwart-witfilms en voor lichtgevoelig papier), met als doel het zilverion in zilverhalogeniden te reduceren tot zwart metallisch zilver.
Verder wordt hydrochinon gebruikt als stabilisator voor verven, lakken, vernissen en dergelijk meer. Het dient als inhibitor of antioxidans en wordt aangewend bij de synthese van andere chemische stoffen, zoals andere stabilisatoren, inhibitoren of kleurstoffen.
Hydrochinon wordt ook verwerkt in cosmetica, bijvoorbeeld in huidcrèmes (om een lichtere huidskleur te verkrijgen). Omdat het bij proefdieren onder andere leukemie en huidkanker veroorzaakte, mag dit alleen nog op recept.[2]
Toxicologie en veiligheid
Hydrochinon wordt door het IARC niet beschouwd als kankerwekkende stof voor de mens, omdat er onvoldoende bewijsmateriaal voorhanden is. Bij dieren is er op basis van dierproeven slechts miniem bewijs gevonden dat het carcinogeen zou zijn.[3] De stof is zeer giftig voor in het water levende organismen.
Zie ook
Externe links
Bronnen, noten en/of referenties
|