Vanadium(IV)chloride
Vanadium(IV)chloride (VCl4) is een anorganische verbinding van vanadium. Het is een helderrode vloeistof, die, zoals vanadiumoxytrichloride, hydrolyseert in contact met lucht tot waterstofchloride (HCl).
Vanadium(IV)chloride
| ||||
| Structuurformule en molecuulmodel | ||||
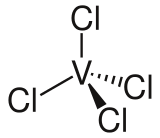 | ||||
Structuurformule van vanadiumtetrachloride | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | VCl4 | |||
| IUPAC-naam | vanadium(IV)chloride | |||
| Molmassa | 192,75 g/mol | |||
| CAS-nummer | 7632-51-1 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H301+H311+H331 - H314 | |||
| EUH-zinnen | EUH014 | |||
| P-zinnen | P261 - P280 - P301+P310 - P305+P351+P338 - P310 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | rood | |||
| Dichtheid | 1,816 g/cm³ | |||
| Smeltpunt | −28 °C | |||
| Kookpunt | 154 °C | |||
| Goed oplosbaar in | water, chloroform | |||
| Geometrie en kristalstructuur | ||||
| Dipoolmoment | 0 D | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Toepassingen
Vanadium(IV)chloride wordt in organische synthese gebruikt om fenolen te koppelen, waarbij er onder andere vanadium(III)chloride (VCl3) wordt gevormd:
This article is issued from
Wikipedia.
The text is licensed under Creative
Commons - Attribution - Sharealike.
Additional terms may apply for the media files.