Tributylfosfaat
Tributylfosfaat of TBP (van het Engelse: tributyl phosphate) is een organische verbinding met als brutoformule C12H27O4P. De stof komt voor als een kleurloze en reukloze viskeuze vloeistof, die slecht oplosbaar is in water.
Tributylfosfaat
| ||||
| Structuurformule en molecuulmodel | ||||
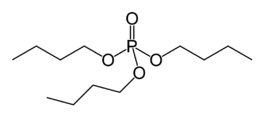 | ||||
Structuurformule van tributylfosfaat | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C12H27O4P | |||
| IUPAC-naam | tributylfosfaat | |||
| Andere namen | tri-n-butylfosfaat, butylfosfaat, fosforzure tributylester | |||
| Molmassa | 266,314141 g/mol | |||
| SMILES | CCCCOP(=O)(OCCCC)OCCCC | |||
| InChI | 1S/C12H27O4P/c1-4-7-10-14-17(13,15-11-8-5-2)16-12-9-6-3/h4-12H2,1-3H3 | |||
| CAS-nummer | 126-73-8 | |||
| EG-nummer | 204-800-2 | |||
| PubChem | 31357 | |||
| Beschrijving | Kleurloze en reukloze vloeistof | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H302 - H315 - H351 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P281 | |||
| EG-Index-nummer | 015-014-00-2 | |||
| ADR-klasse | Gevarenklasse | |||
| MAC-waarde | 1 ppm 11 mg/m³ | |||
| LD50 (ratten) | (oraal) 3000 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos | |||
| Dichtheid | 0,9727 g/cm³ | |||
| Smeltpunt | < −80 °C | |||
| Kookpunt | 289 °C | |||
| Vlampunt | (open vat) 146 °C | |||
| Zelfontbrandings- temperatuur | 410 °C | |||
| Dampdruk | (bij 177°C) 17.000 Pa | |||
| Slecht oplosbaar in | water | |||
| log(Pow) | 4,0 | |||
| Thermodynamische eigenschappen | ||||
| ΔfH | −1380 kJ/mol | |||
| ΔfH | −1454 kJ/mol | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Tributylfosfaat wordt bereid door een verestering van fosforzuur met 1-butanol. Op laboratoriumschaal kan het bereid worden vanuit fosforylchloride:[1]
Toepassingen
Tributylfosfaat is een veelgebruikte weekmaker voor cellulose-esters, zoals nitrocellulose en celluloseacetaat. Het vormt stabiele hydrofobe complexen met een aantal metalen. Deze complexen zijn zowel oplosbaar in organische oplosmiddelen als in superkritisch CO2.
Verder is tributylfosfaat een oplosmiddel voor inkt, synthestische harsen, rubbers, lijmen, herbiciden en fungiciden.
Industriële toepassingen tributylfosfaat zijn onder andere:
- als component in hydraulische vloeistoffen voor vliegtuigen
- als oplosmiddel voor de extractie en zuivering van zeldzame aarde-elementen uit ertsen
Toxicologie en veiligheid
Tributylfosfaat ontleedt bij verhitting en bij verbranding, met vorming van giftige dampen, waaronder fosforoxiden. Het reageert met warm water, met vorming van corrosief fosforzuur en butanol. De stof tast sommige kunststoffen, rubber en coatings aan.
De stof is sterk irriterend voor de ogen, de huid en de luchtwegen.
Externe links

- (en) Gegevens van Tributylfosfaat in de GESTIS-stoffendatabank van het Duitse Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA) (JavaScript vereist)
Bronnen, noten en/of referenties
|

