Scandiumoxide
Scandiumoxide is het oxide van scandium, met als brutoformule Sc2O3. De stof komt voor als een witte kristallijne vaste stof, die onoplosbaar is in water.
Scandiumoxide
| ||||
| Structuurformule en molecuulmodel | ||||
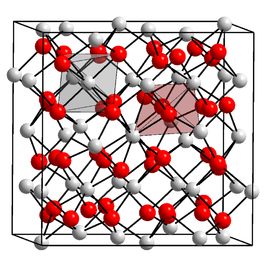 | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | Sc2O3 | |||
| IUPAC-naam | scandiumoxide | |||
| Andere namen | scandiumtrioxide | |||
| Molmassa | 137,91002 g/mol | |||
| SMILES | O=[Sc]O[Sc]=O | |||
| InChI | 1S/3O.2Sc | |||
| CAS-nummer | 12060-08-1 | |||
| PubChem | 4583683 | |||
| Beschrijving | Witte kristallijne vaste stof | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Dichtheid | 3,86 g/cm³ | |||
| Smeltpunt | 2485 °C | |||
| Onoplosbaar in | water | |||
| Geometrie en kristalstructuur | ||||
| Kristalstructuur | kubisch | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Kristalstructuur en eigenschappen
Scandiumoxide kristalliseert uit in een kubisch kristalstelsel. Het behoort tot ruimtegroep 1a3-Th. De lengte van een zijde van de eenheidscel bedraagt 985 pm.
Scandiumoxide is een amfoteer oxide: het lost op in zowel zuren als basen. In een overmaat zoutzuur wordt het omgezet tot scandiumchloride:
In oplossingen van alkali-metalen worden scandaat-zouten gevormd. Een voorbeeld is de reactie van scandiumoxide met kaliumhydroxide, waarbij kaliumhexahydroxoscandaat(III) (K3Sc(OH)6) wordt gevormd.
Door reactie met trifluormethaansulfonzuur wordt scandiumtrifluormethaansulfonaat gevormd, een Lewis-zuur.
Toepassingen
Scandiumoxide wordt, wegens het hoge smeltpunt, gebruikt in systemen die tegen hoge temperaturen en grote temperatuurschommelingen moeten bestand zijn. Verder wordt het verwerkt in keramiek en glas.