Ammoniumbromide
Ammoniumbromide (NH4Br) is het ammoniumzout van waterstofbromide. Het is een kleurloze of witte kristallijne vaste stof die goed oplosbaar is in water. In water dissocieert het in ammonium- en bromide-ionen. De oplosbaarheid is groter in warm water: bij 100 °C is de oplosbaarheid 1456 g/L.[1] Ammoniumbromide is reukloos en heeft een sterke zoutsmaak. Het is een weinig hygroscopisch en als het aan de lucht is blootgesteld wordt het langzaam geel. Bij verhitting sublimeert het en ontleedt het uiteindelijk in ammoniak en waterstofbromide. Ammoniumbromide is niet ontvlambaar. Het is irriterend voor de ogen.
Ammoniumbromide
| ||||
| Structuurformule en molecuulmodel | ||||
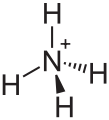 | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | NH4Br | |||
| Molmassa | 97,94 g/mol | |||
| CAS-nummer | 12124-97-0 | |||
| EG-nummer | 235-183-8 | |||
| PubChem | 25514 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H319 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P305+P351+P338 | |||
| LD50 (ratten) | (oraal) 2714 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos | |||
| Dichtheid | 2,43 g/cm³ | |||
| Sublimatiepunt | 452 °C | |||
| Oplosbaarheid in water | 970 g/l | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Ammoniumbromide wordt gevormd door dibroom met een overmaat ammoniak te reageren:
Een alternatief is de rechtstreekse reactie van ammoniak met waterstofbromide:
Ammoniumbromide wordt ook geproduceerd door de reactie van ammoniak met een oplossing van ijzerbromiden, die men bekomt door een broomoplossing in contact te brengen met ijzervijlsel:
Ammoniumbromide wordt onder meer geproduceerd bij ICL-IP Terneuzen BV in Terneuzen, het vroegere Broomchemie.
Toepassingen[2]
Ammoniumbromide wordt in de (analoge) fotografie gebruikt bij de bereiding van lichtgevoelige emulsies voor fotografische film, papier of platen en van ontwikkelaar- en fixeerbaden. Het wordt gebruikt om hout vuurbestendig te maken, en als vlamvertragend additief voor onder meer celluloseacetaat en andere cellulose-esters.[3]
Ammoniumbromide wordt ook verwerkt in corrosie-inhibitoren en in geneeskundige preparaten, maar deze laatste toepassing wordt niet meer aangeraden.[1]
Bronnen, noten en/of referenties
|
