Alcohol (stofklasse)
Een alcohol of ook wel alkanol en vroeger carbinol genoemd, is in de scheikunde een organische verbinding met een hydroxylgroep gebonden met organische koolstofketen (een aryl- of alkylgroep). Het woord alcohol is afgeleid van het Arabische woord al-kuḥl (الكحل).[1] Onverzadigde ketens waarbij een hydroxylgroep rechtstreeks op een dubbele binding is gebonden, worden enolen genoemd. Zij tautomeriseren echter snel naar het stabiele keton.
De eenvoudigste alcohol is methanol (CH3OH). De bekendste alcohol is ethanol (C2H5OH). Als in het dagelijks leven van 'alcohol' sprake is, wordt doorgaans ethanol bedoeld. In de vroegere naamgeving krijgt het alkanol de naam van de alkaangroep als achtervoegsel -yl + alcohol. Zo zijn methylalcohol en ethylalcohol verouderde namen voor respectievelijk methanol en ethanol, maar ze worden nog weleens gebruikt.
Alcoholen kunnen een reactie aangaan met carbonzuren of anorganische zuren. Er ontstaat dan een ester. Deze stoffen zijn niet onbelangrijke bouwstenen voor de mens.
Andere alcoholen zijn onder andere
- propanol (1-propanol), CH3CH2CH2OH ; 2-propanol (isopropanol, ook wel bekend als IPA), CH3CHOHCH3
- butanol; isobutanol
- etheenglycol, een alkaandiol
- glycerine, een alkaantriol
- polyolen als mannitol en sorbitol
Indeling
Alcoholen kunnen onderverdeeld worden in:
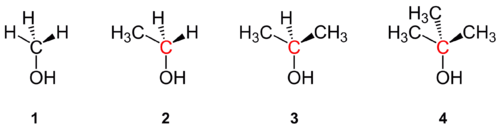
- Primaire alcoholen: een alcohol waarin het koolstofatoom dat de OH-groep draagt aan maximaal één ander koolstofatoom gebonden is heet een primair alcohol.
- Secondaire alcoholen: is het koolstofatoom aan twee andere koolstofatomen gebonden, dan heet het een secundair alcohol.
- Tertiaire alcoholen: is het koolstofatoom aan drie andere koolstofatomen gebonden dan spreekt men van een tertiair alcohol.
Alcoholen als oplosmiddel
Alcoholen kenmerken zich als oplosmiddelen doordat zij doorgaans erg polair zijn, zeker wanneer de restketen kort is. Maar de stoffen laten zich zowel met water als met apolaire stoffen goed mengen, en worden zelf minder hydrofiel naarmate de koolwaterstofketen van het alcoholmolecuul groter wordt.
Reactiviteit van alcoholen
Oxidatiereacties
In de partiële oxidatie van alcoholen blijkt het onderscheid tussen primaire, secundaire en tertiaire alcoholen belangrijk. Primaire alcoholen worden in eerste instantie tot het aldehyde en dan tot het carbonzuur met hetzelfde aantal koolstofatomen (en structuur) geoxideerd, secundaire alcoholen worden tot het keton met hetzelfde koolstofskelet geoxideerd. Tertiaire alcoholen worden onder deze omstandigheden niet geoxideerd. Doorgaans verloopt (partiële) oxidatie van primaire alcoholen in deze volgorde: methylgroep → alcohol/alkanol (hydroxylgroep) → aldehyde/alkanal (carbonylgroep) → carbonzuur (carboxygroep).
Reacties met zuren
Met zuren worden door alkanolen esters gevormd. Carbonzuuresters van primaire alcoholen hebben vaak een fruitachtige geur. De reactie is een evenwichtsreactie waarbij water vrijkomt. Secundaire alcoholen reageren wel, maar minder snel, vaak is het zuuranhydride nodig. Esters van tertiaire alcoholen moeten vaak via een omweg bereid worden; ook hierbij is het zuuranhydride nodig. Halogeenalkanen laten zich behalve door additie-reacties ook vormen door verestering, bijvoorbeeld de vorming van broomethaan uit waterstofbromide en geconcentreerde ethanol onder katalyse van een sterk zuur:
Veresteringsreacties kan men opvatten als een zuur-basereactie, waarbij het alcohol de rol van organische base vervult.
Reacties met metalen
Alcoholen reageren niet of zeer langzaam met de meeste metalen. Een uitzondering wordt gevormd door de alkali- en de aardalkali-metalen. Naast waterstofgas ontstaat een alcoholaat. Ethanol reageert bijvoorbeeld met natrium onder vorming van waterstof en natriumethanolaat:
Toepassingen van deze reactie zijn onder andere:
- Voor speciale reacties noodzakelijke reagentia.
In de malonzuurestersynthese is het noodzakelijk de zelfde alcohol te gebruiken voor het voltooiing van de reactie als die waarmee het malonzuur veresterd is. - Vernietigen van resten van (aard)alkalimetalen.
De reactie van deze metalen met alcoholen is veel rustiger dan de reactie met water. Natrium reageert vaak uiteindelijk[2] explosief met water, met ethanol verloopt de reactie zeer rustig. - Schoonmaak van laboratoriumglaswerk.
Hiervoor wordt het alcoholaat meestal niet speciaal gemaakt, doorgaans is op het betreffende laboratorium regelmatig natrium nodig en moeten er dus regelmatig natriumresten opgeruimd worden.
Zie ook
| Zie de categorie Alcohols van Wikimedia Commons voor mediabestanden over dit onderwerp. |
Bronnen, noten en/of referenties
|