4,4'-bifenol
4,4'-bifenol is een tweewaardig fenol, bestaande uit twee moleculen fenol die met een koolstof-koolstofbinding verbonden zijn. Deze binding verbindt de koolstofatomen op positie 4 (de para-positie) ten opzichte van de hydroxylgroepen. Alternatief kan men de stof beschouwen als een derivaat van bifenyl.
4,4'-bifenol
| ||||
| Structuurformule en molecuulmodel | ||||
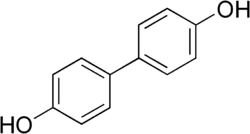 | ||||
Structuurformule van 4,4'-bifenol | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C12H10O2 | |||
| IUPAC-naam | bifenyl-4,4'-diol | |||
| Andere namen | 4,4'-dihydroxybifenyl | |||
| Molmassa | 186,21 g/mol | |||
| CAS-nummer | 92-88-6 | |||
| EG-nummer | 202-200-5 | |||
| Beschrijving | Lichtgrijs reukloos poeder | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H312 - H315 - H319 - H335 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P261 - P280 - P305+P351+P338 | |||
| LD50 (ratten) | (oraal) 4920[1] mg/kg | |||
| LD50 (konijnen) | (dermaal) 1780[1] mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | lichtgrijs | |||
| Smeltpunt | 278-283 °C | |||
| Kookpunt | (ontbindt) °C | |||
| Oplosbaarheid in water | < 0,01 g/l | |||
| Goed oplosbaar in | ethanol, di-ethylether | |||
| Slecht oplosbaar in | water | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
De stof wordt ook bifenol genoemd. Men mag bifenol niet verwarren met bisfenol zoals in bisfenol A.
Synthese
De eerste gepubliceerde synthese van bifenyl bestond uit de ontbinding van de corresponderende diazoverbinding (gevormd uit benzidine en nitriet), opgelost in geconcentreerd zwavelzuur.[2]
Tegenwoordig wordt bifenyl voornamelijk bereid uitgaande van 2,6-di-tert-butylfenol. Dit wordt eerst gedimeriseerd met behulp van zuurstof en een sterke base als katalysator (natriumhydroxide of kaliumhydroxide). Het bekomen dimeer wordt geoxideerd tot de chinonvorm en wordt daarom met waterstofgas gereduceerd tot het corresponderende 3,3',5,5'-tetra-tert-butylbifenol. Ten slotte worden de tertiaire butylgroepen verwijderd (dealkylering) door verhitting tot ca. 330 °C, waarbij er isobuteen ontwijkt en 4,4'-bifenol overblijft.[3]
Toepassingen
- Als antioxidant
- Als intermediaire stof in de synthese van verfstoffen
- Als co-monomeer voor polymeren. Bifenol is een diol en kan reageren met fosgeen, dibasische zuren, di-isocyanaten en dergelijke tot polycarbonaten, polyurethanen, polyesters en andere polymeren. Met bifenol kunnen volledig aromatische polymeren gemaakt worden die mechanisch sterk zijn, bestand tegen hoge temperatuur en een goede weerstand tegen oxidatie en solventen hebben.
Gevaren
Bifenol veroorzaakt irritatie van ogen, huid en luchtwegen. Het is schadelijk bij absorptie door de huid.
Bronnen, noten en/of referenties
|
