Swern-oxidatie
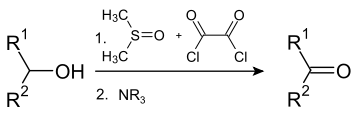
De Swern-oxidatie, ontdekt door Daniel Swern, is een zeer selectieve en milde methode voor de oxidatie van primaire of secundaire alcoholen tot respectievelijk aldehyden of ketonen.[1] De organische reactie wordt uitgevoerd met oxalylchloride, dimethylsulfoxide en tri-ethylamine.
Grote voordelen van deze milde methode zijn de hoge selectiviteit: in tegenstelling tot andere oxidaties (zoals de Jones-oxidatie) wordt een aldehyde niet verder geoxideerd tot een carbonzuur. De reactietemperatuur bedraagt tussen -78 en 20 °C. Een bijkomend voordeel ten opzichte van de chroom(IV)verbindingen die normaliter gebruikt worden voor oxidaties, is de geringe toxiciteit van de reagentia.
Reactiemechanisme
De eerste stap van de Swern-oxidatie bestaat erin dimethylsulfoxide te activeren door reactie van een van beide resonantiestructuren (1b) met oxalylchloride (2) tot een sulfoxonium-intermediair (3). Dit intermediair ontleedt snel tot koolstofdioxide en koolstofmonoxide, waardoor het dimethylchloorsulfoniumchloride (4), het geactiveerde dimethylsulfoxide, wordt gevormd.

Vervolgens wordt het alcohol (5) toegevoegd aan dit dimethylchloorsulfoniumchloride, waardoor een intermediaire alkoxysulfoniumverbinding (6) ontstaat. Door toevoeging van ten minste 2 equivalenten van een organische base (doorgaans tri-ethylamine) ontstaat een zwavelylide (7). Dit ylide kan via een cyclische transitietoestand ontleden tot dimethylsulfide (een gas) en de uiteindelijke carbonylverbinding (8).

Zie ook
Bronnen, noten en/of referenties
|