Perchloraat
Perchloraat is een oxoanion met als brutoformule ClO4−. Perchloraten zijn zout van perchloorzuur.
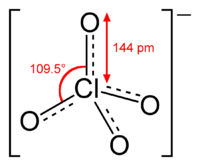

Structuur
Het perchloraation heeft de vorm van een tetraëder, de vier chloor-zuurstofbindingen hebben een gelijke lengte. Het chlooratoom bevindt zich in hoogste oxidatietoestand en heeft een formele lading van +7.
Eigenschappen
Perchloraten zijn in het algemeen goed oplosbaar in waterige oplossingen en worden daarom in chemisch onderzoek veel gebruikt om kationen in oplossing te brengen die met andere tegenionen niet in oplossing te brengen zijn. Het ion is een sterke oxidator en moet met omzichtigheid behandeld worden omdat bij verhitting in droge vorm ontleding optreedt met de vorming van gasvormige producten. Explosies zijn daarbij niet uit te sluiten. In waterige oplossingen is de pH van invloed op de grootte van het oxiderend vermogen.
Het perchloraat-ion is een van de zwakste basen.
Perchloraten
- Ammoniumperchloraat, NH4ClO4
- Cesiumperchloraat, CsClO4
- Lithiumperchloraat, LiClO4
- Magnesiumperchloraat, Mg(ClO4)2
- Perchloorzuur, HClO4
- Kaliumperchloraat, KClO4
- Rubidiumperchloraat, RbClO4
- Zilverperchloraat, AgClO4
- Natriumperchloraat, NaClO4