Methyltrifluormethaansulfonaat
Methyltrifluormethaansulfonaat of methyltriflaat is de methylester van het superzuur trifluormethaansulfonzuur.
Methyltrifluormethaansulfonaat
| ||||
| Structuurformule en molecuulmodel | ||||
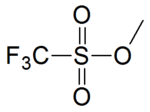 | ||||
Structuurformule van methyltrifluormethaansulfonaat | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C2H3F3O3S | |||
| IUPAC-naam | methyltrifluormethaansulfonaat | |||
| Andere namen | methyltriflaat | |||
| Molmassa | 164,1 g/mol | |||
| CAS-nummer | 333-27-7 | |||
| EG-nummer | 206-371-7 | |||
| Beschrijving | Kleurloze tot gele vloeistof | |||
| Vergelijkbaar met | dimethylsulfaat, trimethyloxoniumtetrafluorboraat | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H226 - H314 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P280 - P305+P351+P338 - P310 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos-geel | |||
| Dichtheid | 1,45 g/cm³ | |||
| Kookpunt | 95 °C | |||
| Vlampunt | 38 °C | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Toepassingen
Methyltrifluormethaansulfonaat is een zeer efficiënt methyleringsreagens in de organische chemie, omdat het zo'n 10.000 tot 100.000 keer reactiever is dan methyltosylaat of methyljodide.[1] Het kan een alternatief vormen voor dimethylsulfaat, dat giftig en mogelijk kankerverwekkend is. Methyltrifluormethaansulfonaat wordt onder meer gebruikt voor de methylering van koolhydraten[2][3] en van aminozuren.[4]
Toxicologie en veiligheid
Methyltrifluormethaansulfonaat is een gevaarlijke stof: contact ermee veroorzaakt brandwonden bij alle blootstellingswijzen (met huid of ogen, bij inademing of ingestie). Zowel de vloeistof als de damp is ontvlambaar. De stof is incompatibel met sterke oxidatoren, sterke reductoren, zuren en basen.
Externe links
Bronnen, noten en/of referenties
|