Methaansulfonzuur
Methaansulfonzuur is het eenvoudigste alkylsulfonzuur, met als brutoformule CH4SO3. Het is een kleurloze corrosieve vloeistof.
Methaansulfonzuur
| ||||
| Structuurformule en molecuulmodel | ||||
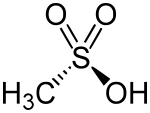 | ||||
Structuurformule van methaansulfonzuur | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | CH4O3S | |||
| IUPAC-naam | methaansulfonzuur | |||
| Molmassa | 96,11 g/mol | |||
| SMILES | CS(=O)(=O)O | |||
| CAS-nummer | 75-75-2 | |||
| EG-nummer | 200-898-6 | |||
| PubChem | 6395 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H314 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P280 - P305+P351+P338 - P310 | |||
| EG-Index-nummer | 607-145-00-4 | |||
| VN-nummer | 2922 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,48 g/cm³ | |||
| Smeltpunt | 20 °C | |||
| Kookpunt | (bij 13 hPa) 167 °C | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Esters of zouten van methaansulfonzuur worden mesylaten genoemd.
Synthese
Methaansulfonzuur wordt bereid door de hydrolyse van methaansulfonylchloride, dat men bekomt door de oxidatie van methaanthiol. Het kan ook bereid worden door de reactie van methaanthiol met waterstofperoxide in oplossing, waarbij het zuur zelf als katalysator optreedt.[1]
Een alternatieve bereidingswijze is de reactie van azijnzuur met zwaveldioxide en zuurstofgas, die opgaat door bestraling met licht met een golflengte tussen 240 en 320 nm. Naast methaansulfonzuur ontstaat daarbij ook zwavelzuur.[2]
Toepassingen
Methaansulfonzuur wordt toegepast bij elektroplating. Daarnaast fungeert het als katalysator van alkyleringen, veresteringen of polymerisaties, en als solvent of als oppervlakteactieve stof.
Externe links
| Bronnen, noten en/of referenties |