Fluor-18
Fluor-18 of 18F is een onstabiele radioactieve isotoop van fluor, een halogeen. De isotoop komt van nature niet op Aarde voor.
Fluor-18
| ||||
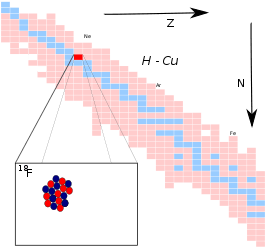 | ||||
Fluor-18 op de isotopenkaart | ||||
| Algemeen | ||||
| Element | fluor (F) | |||
| Nuclide | 18F | |||
| Aantal protonen | 9 | |||
| Aantal neutronen | 9 | |||
| Nuclidische gegevens | ||||
| Nuclidenmassa | 18,000937956 u | |||
| Spin | 1+ | |||
| Bindingsenergie | 7,631605 MeV | |||
| Massa-overschot | 0,873701 MeV | |||
| Vervalgegevens | ||||
| Type verval | β+-verval | |||
| Halveringstijd | 109,771 minuten | |||
| Vervalenergie | 633,023 keV | |||
| Vervalproduct | zuurstof-18 | |||
| Isotopen van fluor | ||||
| ||||
Fluor-18 ontstaat bij het radioactief verval van neon-18.
Radioactief verval
Fluor-18 vervalt middels β+-verval tot de stabiele isotoop zuurstof-18:
De halveringstijd bedraagt 109,771 minuten.
Toepassingen
Het radioactief verval van fluor-18 wordt gebruikt in de nucleaire geneeskunde (bij medische beeldvorming aan de hand van positronemissietomografie). Zuurstof-18-verrijkt water wordt in een cyclotron of een andere deeltjesversneller gebombardeerd met waterstofionen, zodat fluor-18 ontstaat. Deze isotoop wordt ingebouwd in fluordeoxyglucose, dat aan de patiënt wordt toegediend. 18F-Florbetapir is zo'n middel dat wordt geïnjecteerd voor het maken van een PET-scan. Fluor-18 kan ook worden ingebouwd in andere tracers zoals in F18-DOPA, dat gebruikt wordt in het onderzoek naar de ziekte van Parkinson.
Bronnen, noten en/of referenties
|
| Isotopen van fluor (F) |
|---|
|
14F · 15F · 16F · 17F · 18F · 19F · 20F · 21F · 22F · 23F · 24F · 25F · 26F · 27F · 28F · 29F · 30F · 31F |