Acetonperoxide
Acetonperoxide of TATP (triacetontriperoxide) is een springstof behorend tot de organische peroxiden. De stof is zeer instabiel: hitte, wrijving, schokken of statische elektriciteit kunnen het doen detoneren. Het gemak waarmee het gemaakt kan worden maakt het bijgevolg bijzonder gevaarlijk. De grondstoffen waterstofperoxide, aceton en geconcentreerd zwavelzuur of zoutzuur zijn gemakkelijk verkrijgbaar bij de meeste bouwmarkten of een apotheek. De synthese-reactievergelijking is als volgt:
Acetonperoxide
| ||||
| Structuurformule en molecuulmodel | ||||
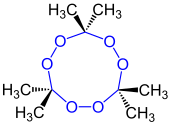 | ||||
Structuurformule van acetonperoxide (trimeer) | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C9H18O6 | |||
| IUPAC-naam | acetonperoxide | |||
| Andere namen | triaceton-triperoxide, TATP, peroxyaceton, tricycloaceton-peroxide, TCAP | |||
| Molmassa | 222,24 g/mol | |||
| SMILES | C1(C)(OOC(C)(OOC(C)(OO1)C)C)C | |||
| CAS-nummer | 17088-37-8 | |||
| Fysische eigenschappen | ||||
| Dichtheid | 1,8 g/cm³ | |||
| Smeltpunt | 91 °C | |||
| Dampdruk | (bij 30°C) 6,46[1] Pa | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Het is ook bekend onder de namen triaceton-triperoxide (TATP), peroxyaceton en tricycloaceton-peroxide (TCAP). In feite bestaan er drie varianten: diaceton-diperoxide (de dimeer), triacetontriperoxide (de trimeer) en een tetrameer, die zich vormt met tin(IV)chloride als katalysator.[2] Het dimeer ontploft met minder kracht maar is gevoeliger, de trimeer heeft wat meer kracht maar is iets minder gevoelig. Bij een reactie tussen aceton en waterstofperoxide met een temperatuur boven de 10°C ontstaat vooral de dimeer, bij lagere temperaturen de trimeer. Ook bij lagere temperaturen ontstaat echter altijd een fractie dimeer.
Het explosieve karakter van acetonperoxide is gebaseerd op de desintegratie van de moleculen van triaceton-triperoxide waarbij aceton, zuurstof en ozon vrijkomt (waarvan de aceton vaak nog met de eveneens ontstane zuurstof en ozon verbrandt tot CO2 en water). De overgang van vaste stof naar gas geeft een volumevergroting. Omdat deze expansie zo snel en massaal plaatsvindt, heeft het een explosief karakter. Bij deze chemische reactie komt relatief weinig warmte vrij.
Acetonperoxide sublimeert vrij makkelijk. Deze eigenschap maakt het zeer gevaarlijk de stof in een pot met schroefdop te bewaren: het middel kan sublimeren en neerslaan in het schroefdeksel, zodat het openschroeven kan leiden tot een detonatie.
Bij hoeveelheden van minder dan 2 gram verbrandt acetonperoxide op agressieve wijze, bij grotere hoeveelheden detoneert het. Ook detoneert de stof als deze onder verhoogde druk gebracht wordt. Acetonperoxide detoneert op volgende wijze:
De detonatiesnelheid van acetonperoxide bedraagt 5300 m/s.
Acetonperoxide was het explosieve ingrediënt van bommen van Islamitische Staat, zowel op het slagveld in Syrië als bij terroristische aanslagen in Parijs en Brussel.[3]
Bronnen, noten en/of referenties
|
| Zie de categorie Acetone peroxide van Wikimedia Commons voor mediabestanden over dit onderwerp. |