Zwavelhexafluoride
Zwavelhexafluoride (SF6) is een anorganische verbinding van zwavel met fluor. Het is een kleurloos en geurloos gas, dat in de meeste gevallen chemisch inert is. Zwavelhexafluoride is apolair en dus niet oplosbaar in water, wel in organische oplosmiddelen (benzeen, di-ethylether, ethanol, enzovoort). De dichtheid is ongeveer 5 keer zo hoog als die van lucht.
Zwavelhexafluoride
| ||||
| Structuurformule en molecuulmodel | ||||
 | ||||
Structuurformule van zwavelhexafluoride | ||||
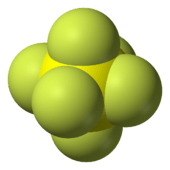 | ||||
Molecuulmodel van zwavelhexafluoride | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | SF6 | |||
| IUPAC-naam | zwavelhexafluoride | |||
| Andere namen | zwavel(VI)fluoride, Elagas, Esaflon | |||
| Molmassa | 146,055419 g/mol | |||
| SMILES | FS(F)(F)(F)(F)F | |||
| InChI | 1S/F6S/c1-7(2,3,4,5)6 | |||
| CAS-nummer | 2551-62-4 | |||
| EG-nummer | 219-854-2 | |||
| PubChem | 17358 | |||
| Beschrijving | Kleurloos gas | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H280 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P410+P403 | |||
| VN-nummer | 1080 | |||
| LD50 (konijnen) | (intraveneus) 5790 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | gasvormig | |||
| Kleur | kleurloos | |||
| Dichtheid | 6,164 × 10−3 g/cm³ | |||
| Sublimatiepunt | −64 °C | |||
| Dampdruk | (bij 21°C) 2900 Pa | |||
| Goed oplosbaar in | organische oplosmiddelen | |||
| Onoplosbaar in | water | |||
| Geometrie en kristalstructuur | ||||
| Dipoolmoment | 0 D | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Zwavelhexafluoride is een sterk broeikasgas, 23.000 keer zo sterk als koolstofdioxide.[1]
Toepassingen
Het heeft toepassingen in de elektrotechniek bij de middenspanning en hoogspanning, omdat het een hogere doorslagspanning heeft dan lucht; in de metaalverwerking (vooral met aluminium en magnesium) en in de medische techniek, vooral omdat het inert is. Door vonken kan zich wel S2F10 vormen, dat extreem giftig is. Het wordt toegepast in de oogheelkunde door dit gas in de oogbol aan te brengen om losgelaten netvlies na operatieve behandeling op zijn plaats te houden. Het gas lost langzaam op in de bloedbaan.
Lage stem
Als het gas wordt ingeademd zal de stem zeer laag klinken. Dit komt doordat zwavelhexafluoride vijf keer zo dicht is als lucht. Het effect is vergelijkbaar met het inademen van helium, wat een kenmerkende hoge heliumstem tot gevolg heeft.[2] Het inhaleren van zwavelhexafluoride is onveilig omdat het gas zo zwaar is, dat het in de longen kan blijven hangen waardoor verstikking dreigt. Ook bij toevoeging van zuurstof geldt dit.
Bronnen, noten en/of referenties
|
