Zilvernitraat
Zilvernitraat (AgNO3) is het zilverzout van salpeterzuur. De stof komt voor als een kleurloze tot witte kristallijne vaste stof, die zeer goed oplosbaar is in water.
Zilvernitraat
| ||||
| Structuurformule en molecuulmodel | ||||
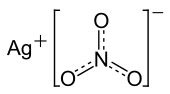 | ||||
Structuurformule van zilvernitraat | ||||
 | ||||
Zilvernitraat-kristallen | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | AgNO3 | |||
| IUPAC-naam | zilvernitraat | |||
| Molmassa | 169,89 g/mol | |||
| SMILES | [N+](=O)([O-])[O-].[Ag+] | |||
| InChI | 1/Ag.NO3/c;2-1(3)4/q+1;-1 | |||
| CAS-nummer | 7761-88-8 | |||
| EG-nummer | 231-853-9 | |||
| PubChem | 24470 | |||
| Beschrijving | Kleurloze kristallen die grijs worden o.i.v. licht | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H314 - H410[1] | |||
| EUH-zinnen | geen | |||
| P-zinnen | P220 - P273 - P280 - P305+P351+P338 - P310 - P501[1] | |||
| Opslag | Bewaren in het donker (product is lichtgevoelig), verwijderd houden van hitte, vonken, open vlammen en brandbare producten | |||
| VN-nummer | 1493 | |||
| ADR-klasse | klasse 5,1 PG II | |||
| MAC-waarde | 0,01 mg/m³ | |||
| LD50 (ratten) | (oraal) 1173 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos tot wit | |||
| Dichtheid | 4,352 g/cm³ | |||
| Smeltpunt | 212 °C | |||
| Kookpunt | (ontleedt) 440 °C | |||
| Oplosbaarheid in water | 2160 g/l | |||
| Goed oplosbaar in | water | |||
| Slecht oplosbaar in | ethanol | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Zilvernitraat kan bereid worden door zilver op te lossen in salpeterzuur:
Het stikstofmonoxide (NO) dat hierbij ontstaat, reageert vervolgens weer met dizuurstof uit de lucht tot stikstofdioxide (NO2). Dit is zichtbaar als bruinrode nitreuze dampen.
Eigenschappen en toepassingen
In tegenstelling tot de zilverhalogeniden AgCl, AgBr en AgI is zilvernitraat een goed oplosbaar zout. Wanneer een zilvernitraatoplossing gevoegd wordt bij een oplossing van natriumchloride (NaCl), slaat het slecht oplosbare zilverchloride neer:
Zilvernitraat wordt ook wel helse steen (lapis infernalis) genoemd. Het ziet eruit als kleurloze, heldere kristallen. In contact met de vochtige huid dringt er zilverzout binnen dat daarna door het licht of anti-oxidanten wordt ontleed, zoals veel zilverzouten (zie fotografie) waarbij er, naast salpeterzuur, fijnverdeeld zilver wordt gevormd. De huid kleurt dan grijs of blauw-grijs, een aandoening die ook wel argyrie genoemd wordt. Het vindt in deze vaste vorm nog wel toepassing bij het aanstippen van wratten of wild vlees. Vroeger werd een oplossing van zilvernitraat gebruikt om in oogjes van pasgeborenen te druppelen (methode van Crédé) ter voorkoming van ophthalmia neonatorum. Dit werkt goed, maar als het flesje te lang open had gestaan, werd de oplossing door verdamping weleens te geconcentreerd, wat tot oogschade kon leiden. Deze preventiemethode is daarom verlaten. Omdat zilvernitraat een adstringerende werking heeft, wordt het ook in geneeskunde gebruikt om afscheiding van lichaamsvloeistoffen tegen te gaan.
Het nitraat is de meest gangbare vorm waarin zilver als een oplosbare verbinding wordt verhandeld en in het laboratorium wordt gebruikt.
Externe links
- (en) MSDS van zilvernitraat
- (en) Gegevens van Zilvernitraat in de GESTIS-stoffendatabank van het Duitse Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA) (JavaScript vereist)
Bronnen, noten en/of referenties
|