Zilverjodide
Zilverjodide (AgI) behoort tot de zogenaamde zilverhalogeniden. Het is een zout met lage oplosbaarheid in water. Zilverjodide is een vaste ionengeleider. Voor AgI zelf is dat het geval bij verhoogde temperaturen. Er is echter een rubidiumzilverjodide waar dat al het geval is bij kamertemperatuur. Het wordt wel toegepast in batterijen.
Zilverjodide
| ||||
| Structuurformule en molecuulmodel | ||||
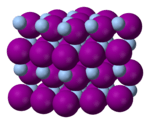 | ||||
Structuur van zilverjodide | ||||
Zilverjodidekristallen | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | AgI | |||
| IUPAC-naam | zilverjodide | |||
| Andere namen | zilvermonojodide, zilver(I)jodide | |||
| Molmassa | 234,77267 g/mol | |||
| SMILES | [Ag]I | |||
| InChI | 1/Ag.HI/h;1H/q+1;/p-1/fAg.I/h;1h/qm;-1 | |||
| CAS-nummer | 7783-96-2 | |||
| EG-nummer | 232-038-0 | |||
| PubChem | 24563 | |||
| Vergelijkbaar met | zilverchloride, zilverbromide | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H410 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P273 - P501 | |||
| Opslag | bewaren in gesloten recipiënt afgesloten van het licht | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | geel | |||
| Dichtheid | 5,67 g/cm³ | |||
| Smeltpunt | 552 °C | |||
| Kookpunt | 1506 °C | |||
| Dampdruk | 466 Pa | |||
| Oplosbaarheid in water | 3 × 10−6 g/l | |||
| Onoplosbaar in | water | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Zilverjodide wordt ook gebruikt om regen te maken.
Toxicologie en veiligheid
Zilverjodide wordt algemeen beschouwd als een schadelijke, vervuilende en toxische verbinding. Inname van jodiden, waaronder zilverjodide, leidt tot huidirritatie, overmatige slijmproductie, hoofdpijn en irritatie van slijmvliezen. Andere symptomen zijn mentale uitputting, bloedarmoede en gewichtsverlies. Chronische inname kan leiden tot argyrie, dat gekenmerkt wordt door het blauwgrijs worden van ogen, huid en slijmvliezen. Chronisch huidcontact kan leiden tot permanente verkleuring van de huid.
