Benzylcyanide
Benzylcyanide (afgekort tot BnCN) of fenylacetonitril is een zeer toxische organische verbinding met als brutoformule C8H7N. De stof komt voor als een kleurloze olieachtige vloeistof met een aromatische geur, die zeer slecht oplosbaar is in water.
Benzylcyanide
| ||||
| Structuurformule en molecuulmodel | ||||
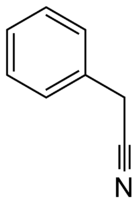 | ||||
Structuurformule van benzylcyanide | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C8H7N | |||
| IUPAC-naam | 2-phenylacetonitrile | |||
| Andere namen | cyanomethylbenzeen, fenylacetonitril, BnCN | |||
| Molmassa | 117,14788 g/mol | |||
| SMILES | C1=CC=C(C=C1)CC#N | |||
| InChI | 1S/C8H7N/c9-7-6-8-4-2-1-3-5-8/h1-5H,6H2 | |||
| CAS-nummer | 140-29-4 | |||
| EG-nummer | 205-410-5 | |||
| PubChem | 8794 | |||
| Beschrijving | Kleurloze olieachtige vloeistof | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H301 - H311 - H330 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P260 - P280 - P284 - P310 | |||
| Opslag | Gescheiden van zuren. Goed gesloten en brandveilig opslaan. | |||
| VN-nummer | 2470 | |||
| ADR-klasse | Gevarenklasse 6.1 | |||
| LD50 (ratten) | (oraal) 270 mg/kg (huid) 2000 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,015 g/cm³ | |||
| Smeltpunt | −24 °C | |||
| Kookpunt | 233-234 °C | |||
| Dampdruk | (bij 20°C) 7 Pa | |||
| Oplosbaarheid in water | (bij 20°C) 1,7 g/l | |||
| Slecht oplosbaar in | water | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Benzylcyanide wordt bereid uit reactie van benzylchloride en natriumcyanide in ethanol via een SN2-reactie.
Toepassingen en reacties
Benzylcyanide is een van de belangrijkste verbindingen met een zogenaamde actieve methyleengroep. Deze kan tal van organische reacties aangaan.
De stof is een belangrijk intermediair in de productie van tal van - meestal toxische - verbindingen. Zo wordt het gebruikt bij de synthese van fenobarbital, methylfenidaat, fenylazijnzuur, methadon, pethidine, ketobemidon en een aantal amfetamines. Verder is benzylcyanide een precursor voor de productie van sibutramine en aanverwante verbindingen.
Toxicologie en veiligheid
Net zoals alle cyaniden, is ook benzylcyanide een zeer toxische verbinding. Immers, bij contact met (sterke) zuren of bij verbranding wordt het zeer toxische blauwzuur gevormd. Het is irriterend voor de ogen en de huid en toxisch bij inhalatie of inslikken.
