Nikkel(II)oxide
Nikkel(II)oxide (NiO) is een anorganische verbinding van het metaal nikkel met zuurstof. Andere nikkeloxiden zijn nikkel(III)oxide (Ni2O3) en nikkel(IV)oxide (NiO2). De stof komt voor als een donkergroene tot zwarte kristallijne vaste stof met een kubische kristalstructuur. Nikkel(II)oxide is een basisch oxide en vrijwel onoplosbaar in water.
Nikkel(II)oxide
| ||||
| Structuurformule en molecuulmodel | ||||
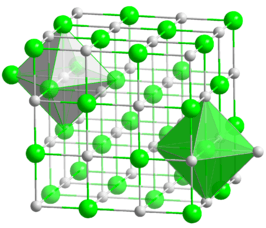 | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | NiO | |||
| IUPAC-naam | nikkel(II)oxide | |||
| Andere namen | nikkelmonoxide | |||
| Molmassa | 74,6928 g/mol | |||
| SMILES | 1S/Ni.O | |||
| InChI | O=[Ni] | |||
| CAS-nummer | 1313-99-1 | |||
| EG-nummer | 215-215-7 | |||
| PubChem | 14805 | |||
| Beschrijving | Donkergroen tot zwart poeder | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H317 - H350 - H372 - H413 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P201 - P280 - P308+P313 | |||
| Carcinogeen | ja | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | donkergroen tot zwart | |||
| Dichtheid | 7,45 g/cm³ | |||
| Smeltpunt | 1984 °C | |||
| Onoplosbaar in | water | |||
| Brekingsindex | 2,1818 (589 nm, 20 °C) | |||
| Geometrie en kristalstructuur | ||||
| Kristalstructuur | kubisch | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Natuurlijk voorkomen
De minerale vorm, bunseniet, is genoemd naar de Duitse scheikundige Robert Bunsen. Bunseniet is een zeldzaam mineraal, dat aangetroffen wordt in het Ertsgebergte nabij Johanngeorgenstadt (Duitsland).[1] De hardheid op de hardheidsschaal van Mohs bedraagt 5,5.
Synthese
Nikkel(II)oxide wordt gevormd wanneer nikkelpoeder met zuurstofgas boven 400 °C wordt verwarmd. Het kan ook bereid worden door een zuurstofhoudend zout van nikkel, zoals nikkel(II)carbonaat of nikkel(II)sulfaat, bij hoge temperaturen (meer dan 1000 °C) te calcineren:
Toepassingen
Nikkel(II)oxide wordt gebruikt bij de productie van keramische materialen en het kleuren van porselein. Het wordt ook gebruikt als grondstof voor de productie van nikkelzouten en nikkelbevattende katalysatoren. Nikkel(II)oxide is ook een component in elektroden van brandstofcellen.
De reactie met chroom(III)oxide en zuurstofgas leidt tot vorming van nikkel(II)chromaat:
Toxicologie en veiligheid
Zoals de meeste nikkelverbindingen wordt nikkel(II)oxide beschouwd als een kankerverwekkende stof (via inhalatie van poeder). Contact met de ogen of de huid kan leiden tot irritatie.
Externe links
Bronnen, noten en/of referenties
|

