Methyltrichloorsilaan
Methyltrichloorsilaan is een organische siliciumverbinding met als brutoformule CH3Cl3Si. De stof komt voor als een kleurloze vloeistof met een scherpe geur, die hevig reageert met water.
Methyltrichloorsilaan
| ||||
| Structuurformule en molecuulmodel | ||||
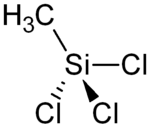 | ||||
Structuurformule van methyltrichloorsilaan | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | CH3Cl3Si | |||
| IUPAC-naam | trichloormethylsilaan | |||
| Andere namen | methylsilicochloroform, monomethyltrichloorsilaan | |||
| Molmassa | 149,47902 g/mol | |||
| SMILES | C[Si](Cl)(Cl)Cl | |||
| InChI | 1S/CH3Cl3Si/c1-5(2,3)4/h1H3 | |||
| CAS-nummer | 75-79-6 | |||
| EG-nummer | 200-902-6 | |||
| PubChem | 6399 | |||
| Beschrijving | Kleurloze vloeistof met scherpe geur | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H225 - H315 - H319 - H335 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P210 - P261 - P305+P351+P338 | |||
| Omgang | Niet roken, niet eten en niet drinken. | |||
| Opslag | Gescheiden van (sterk) oxiderende stoffen, metalen en legeringen. Brandveilig, koel, droog en goed gesloten bewaren. | |||
| EG-Index-nummer | 014-004-00-5 | |||
| VN-nummer | 1250 | |||
| ADR-klasse | Gevarenklasse 3 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,29 g/cm³ | |||
| Smeltpunt | −90 °C | |||
| Kookpunt | 66 °C | |||
| Vlampunt | 8 °C | |||
| Zelfontbrandings- temperatuur | 490 °C | |||
| Dampdruk | (bij 20°C) 17.900 Pa | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Methyltrichloorsilaan wordt samen met dimethyldichloorsilaan en trimethylchloorsilaan bereid door middel van een Müller-Rochowsynthese. Hierbij reageren siliciumpoeder en methylchloride bij een temperatuur van 350°C en met koper als katalysator tot dimethyldichloorsilaan. Deze verbinding disproportioneert verder tot methyltrichloorsilaan en trimethylchloorsilaan:
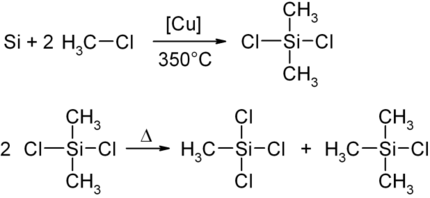 Bereiding van methyltrichloorsilaan uit een disproportioneringsreactie van dimethyldichloorsilaan.
Bereiding van methyltrichloorsilaan uit een disproportioneringsreactie van dimethyldichloorsilaan.
Toxicologie en veiligheid
De stof ontleedt bij verbranding, met vorming van het corrosieve waterstofchloride. Methyltrichloorsilaan reageert hevig met sterk oxiderende stoffen. Ze reageert hevig met water en vochtige lucht, waardoor waterstofchloride wordt gevormd. De stof tast metalen zoals aluminium en magnesium aan.
De stof is corrosief voor de ogen, de huid en de luchtwegen. Inademing van deze stof kan longoedeem veroorzaken. Langdurige of herhaalde blootstelling kan de dood veroorzaken.

