Joodtrichloride
Joodtrichloride is een interhalogeenverbinding met als brutoformule ICl3. Het is een geelbruine vaste stof met een prikkelende geur, die voorkomt als een planair dimeer: I2Cl6. Hierbij dienen twee chlooratomen als brug tussen de joodatomen.[1]
Joodtrichloride
| ||||
| Structuurformule en molecuulmodel | ||||
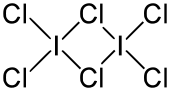 | ||||
Structuurformule van joodtrichloride (dimeer) | ||||
 | ||||
Joodtrichloride-poeder | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | ICl3 | |||
| IUPAC-naam | joodtrichloride | |||
| Molmassa | 233,26347 g/mol | |||
| SMILES | ClI(Cl)Cl | |||
| InChI | 1S/Cl3I/c1-4(2)3 | |||
| CAS-nummer | 865-44-1 | |||
| EG-nummer | 212-739-8 | |||
| PubChem | 70076 | |||
| Beschrijving | Geelbruine vaste stof | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H272 - H314 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P220 - P280 - P305+P351+P338 - P310 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | geelbruin | |||
| Dichtheid | 3,12 g/cm³ | |||
| Smeltpunt | 33 °C | |||
| Kookpunt | (ontleedt) 77 °C | |||
| Goed oplosbaar in | di-ethylether, ethanol, benzeen | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Joodtrichloride kan bereid worden door reactie van di-joodkristallen met vloeibaar chloor bij −70 °C:
Het kan ook bereid worden door een overmaat dichloor toe te voegen aan joodmonochloride:
Eigenschappen en reacties
Gesmolten joodtrichloride is geleidend voor elektrische stroom, wat erop wijst dat er mogelijk dissociatie optreedt:[2]
Joodtrichloride heeft oxiderende eigenschappen. Het reageert hevig met water, onder vorming van zoutzuur, joodmonochloride en waterstofjodaat:
Bronnen, noten en/of referenties
|
This article is issued from
Wikipedia.
The text is licensed under Creative
Commons - Attribution - Sharealike.
Additional terms may apply for the media files.