Hexachloordisilaan
Hexachloordisilaan (Si2Cl6) is een halogenide van silicium.
Hexachloordisilaan
| ||||
| Structuurformule en molecuulmodel | ||||
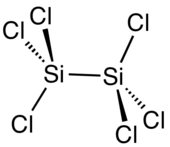 | ||||
Structuurformule van hexachloordisilaan | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | Si2Cl6 | |||
| IUPAC-naam | Hexachloordisilaan | |||
| Molmassa | 268,889 g/mol | |||
| SMILES | [Si]([Si](Cl)(Cl)Cl)(Cl)(Cl)Cl | |||
| InChI | 1S/Cl6Si2/c1-7(2,3)8(4,5)6 | |||
| CAS-nummer | 13465-77-5 | |||
| EG-nummer | 236-704-1 | |||
| PubChem | 83497 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H314 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P280 - P305+P351+P338 - P310 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,562 g/cm³ | |||
| Smeltpunt | −1 °C | |||
| Kookpunt | 144-145 °C | |||
| Vlampunt | 78 °C | |||
| Brekingsindex | 1,475 (589 nm, 20 °C) | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Hexachloordisilaan ontstaat door de reactie van calciumsilicide met chloorgas bij 230 tot 250 °C:
Hierbij ontstaat niet alleen hexachloordisilaan maar een mengsel van gechloreerde oligosilanen van het type SinCl2n+2, met n = 2-6.
Hexachloordisilaan is ook een bijproduct van de productie van trichloorsilaan. Het moet dan uit het reactieproduct afgescheiden worden.
Hexachloordisilaan kan eveneens bekomen worden door een plasma van gasvormig siliciumtetrachloride in aanwezigheid van waterstof te vormen door middel van elektrische wisselstroom met voldoend hoge frequentie. In dit plasma vinden homolytische splitsingen in vrije radicalen plaats, die combineren tot nieuwe verbindingen. Als reactieproduct verkrijgt men een mengsel van hexachloordisilaan en hogere gechloreerde silanen.[1]
Eigenschappen
Het is een kleurloze vloeistof die stabiel is, maar gevoelig voor vocht. Ze reageert heftig met water en reageert met sterke basen, zuren en oxiderende stoffen.
Toepassingen
Hexachloordisilaan wordt gebruikt in de elektronische industrie voor chemical vapor deposition van siliciumhoudende dunne lagen. Daarbij wordt een mengsel van gasvormig hexachloordisilaan en andere gassen als distikstofoxide en ammoniak bij een hoge temperatuur (tot circa 800 °C) over een substraat geleid. Als dragergas fungeert waterstof of stikstof. Op die manier kan men dunne lagen met siliciumdioxide (SiO2) of siliciumoxynitride (SiON) deponeren.[2][3]
Hexachloordisilaan wordt ook gebruikt voor de productie van epitaxiale lagen van silicium.[4]
Hexachloordisilaan is verder een reagens voor de vorming van organosilanen. Het reageert met koolwaterstofhalogeniden volgens de algemene reactie:
Met allylchloride vormt het allyltrichloorsilaan, en met chloorethaan wordt ethyltrichloorsilaan gevormd.[5]
Bronnen, noten en/of referenties
|