Fluorkoolstof
Zie Organofluorchemie voor een meer algemene bespreking van organische fluorverbindingen.
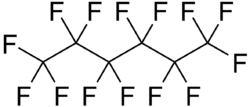
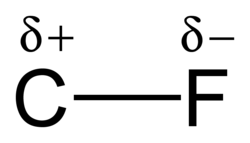
Fluorkoolstoffen, soms ook perfluorkoolstoffen, zijn organische verbindingen die bestaan uit een koolwaterstofketen, waarvan alle waterstofatomen vervangen zijn door fluoratomen.
Fluoralkanen
Fluoralkanen zijn alkanen waarvan de waterstofatomen zijn vervangen door fluoratomen. De koolstof-fluor-binding heeft een van de grootste bindingsenthalpieen van alle enkelvoudige bindingen. De resulterende molecule is daardoor chemisch zeer inert.[1]
Fluoralkenen en fluoralkynen
Omdat er bij alkenen en alkynen respectievelijk een dubbele en drievoudige binding voorkomen, zijn deze fluorkoolstoffen minder stabiel. Een voorbeeld van de instabiliteit is difluorethyn, die erg snel en gemakkelijk polymeriseert tot polytetrafluoretheen (PTFE).[2] Het is bovendien erg reactief ten opzichte van nucleofielen en in een oplossing hydroliseert de stof snel.
Voorbeelden
Fluoralkanen
- Teflon (polytetrafluoretheen)
- Tetrafluormethaan
- Perfluordecaline
Fluoralkenen
- Hexafluorpropeen
- Octafluorcyclobutaan
- Perfluoroisobuteen
- Tetrafluoretheen
Fluoralkynen
- Difluorethyn
Fluorkoolstofderivaten
Derivaten van fluorkoolstoffen zijn afgeleide stoffen van de 'normale' fluorkoolstoffen. Een groot aantal derivaten zijn oppervlakte-actieve stoffen, zoals perfluoroctaanzuur, die helpen bij het vormen van fluoralkanen.
Een andere functie van fluorkoolstofderivaten is als een anestheticum, zoals enfluraan, isofluraan, sevofluraan en desfluraan.
Milieuschade
Fluorverbindingen zijn veelal schadelijk voor het milieu, alhoewel sommige fluorkoolstoffen en fluorkoolstofderivaten in natuurlijke materialen zijn teruggevonden (onder andere in stollingsgesteente en metamorf gesteente).
| Bronnen, noten en/of referenties |