Bariumfluoride
Bariumfluoride (BaF2) is het bariumzout van waterstoffluoride. De stof komt voor als kleurloze kubische kristallen, die slecht oplosbaar zijn in water. Het komt in de natuur voor als het mineraal frankdicksoniet.
Bariumfluoride
| ||||
| Structuurformule en molecuulmodel | ||||
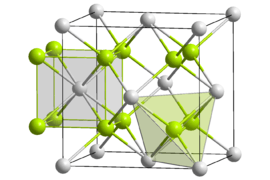 | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | BaF2 | |||
| IUPAC-naam | bariumfluoride | |||
| Andere namen | bariumdifluoride | |||
| Molmassa | 175,323806 g/mol | |||
| SMILES | [F-].[F-].[Ba+2] | |||
| InChI | 1S/Ba.2FH/h;2*1H/q+2;;/p-2 | |||
| CAS-nummer | 7787-32-8 | |||
| EG-nummer | 232-108-0 | |||
| PubChem | 62670 | |||
| Beschrijving | Kleurloze kristallen | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H302 - H332 | |||
| EUH-zinnen | geen | |||
| P-zinnen | geen | |||
| MAC-waarde | 1 mg/m³ | |||
| LD50 (ratten) | (oraal) 250 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos | |||
| Dichtheid | 4,89 g/cm³ | |||
| Smeltpunt | 1355 °C | |||
| Kookpunt | 2260 °C | |||
| Oplosbaarheid in water | 1,2 g/l | |||
| Goed oplosbaar in | methanol, ethanol | |||
| Slecht oplosbaar in | water | |||
| Brekingsindex | 1,46 (589 nm, 20 °C) | |||
| Geometrie en kristalstructuur | ||||
| Kristalstructuur | kubisch | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Bariumfluoride kan bereid worden door de metathesereactie van bariumnitraat en natriumfluoride. Het slecht oplosbare bariumfluoride slaat dan neer:
Het ontstaat ook als nevenproduct bij de thermolyse van bariumhexafluorsilicaat:
Toepassingen
Eenkristallen van bariumfluoride zijn over een wijd bereik van golflengten (150 nm tot 15 μm) transparant, waardoor het in talrijke optische toepassingen kan worden aangewend. Daarnaast doet het dienst als fluxmiddel in de metallurgie voor de zuivering van lichte metalen en de bereiding van legeringen.
Externe links
- (en) Gegevens van Bariumfluoride in de GESTIS-stoffendatabank van het Duitse Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA) (JavaScript vereist)
- (en) MSDS van bariumfluoride
This article is issued from
Wikipedia.
The text is licensed under Creative
Commons - Attribution - Sharealike.
Additional terms may apply for the media files.
