Radialeen
Radialenen vormen een klasse van alicyclische onverzadigde koolwaterstoffen. Ze bestaan uit een cycloalkaan waarbij elk koolstofatoom in de ring een exocyclische dubbele binding bezit. De dubbele bindingen zijn alkeengroepen (C=C), maar derivaten met een carbonylgroep (C=O), of waarin een of meerdere =CH2-groepen zijn vervangen door een ander heteroatoom als zwavel of door een functionele groep met een heteroatoom, zoals stikstof in imine of fosfor,[1] worden ook radialenen genoemd. Het eerste radialeen, hexamethyl[6]radialeen, werd bereid door Hopff en Wick in 1961.[2]
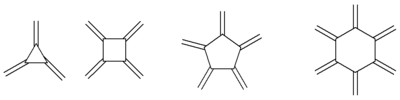
Het kleinste radialeen is trimethyleencyclopropaan of [3]-radialeen. De niet-gesubstitueerde [3]-, [4]- en [6]-radialenen zijn beschreven in de chemische literatuur. De eerste succesvolle synthese van [5]-radialeen werd in 2015 beschreven.[3] Hogere radialenen vanaf [7]-radialeen zijn nog niet bereid. De niet-gesubstitueerde radialenen zijn onstabiel in contact met de lucht en polymeriseren reeds bij kamertemperatuur. Er zijn echter vele stabiele derivaten van deze verbindingen gekend, die eveneens tot de radialenen worden gerekend.
Synthese
De synthese van radialenen gebeurt meestal uitgaande van gesubstitueerde cycloalkanen.
[3]-radialeen of trimethyleencyclopropaan werd bereid uitgaande van 2,3-bis(broommethyl)-1-methyleencyclopropaan.[4]
Niet-gesubstitueerd [4]-radialeen of tetramethyleencyclobutaan (dat bij blootstelling aan de lucht polymeriseert) is bereid via een eliminatiereactie van tetra(broommethyl)cyclobutaan met natriummethanolaat in ethanol. De hydrogenering ervan, gekatalyseerd door platinum op actieve kool, levert tetramethylcyclobutaan:[5]
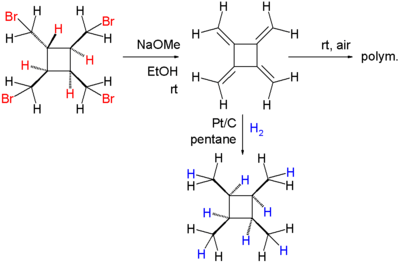
Een andere syntheweg van radialenen is door cyclo-oligomerisatie van [n]-cumulenen. Zo kan [4]-radialeen gevormd worden door de cyclodimerisatie van butatrieen ([3]-cumuleen).[6]
De synthese van [5]-radialeen, C10H10, gebeurde door de decomplexatie bij lage temperatuur van een stabiel organometaalcomplex, [5]radialeen-bis-Fe(CO)3.[3]
Structuur en eigenschappen
Radialenen vertonen bijzondere eigenschappen die theoretisch en experimenteel zijn onderzocht. Alle koolstofatomen in de centrale cycloalkaanring van een radialeen zijn sp2-gehybridiseerd, maar de ring is uitgesproken niet-aromatisch. Dit is een gevolg van het feit dat de dubbele bindingen op de ring niet allemaal tegelijkertijd in conjugatie kunnen staan: dit fenomeen staat bekend als kruisconjugatie (in het Engels cross conjugation). [3]- en [4]-radialenen hebben meestal een vlakke conformatie. [5]-radialenen zoals decamethyl[5]radialeen nemen een halve stoel-conformatie aan, terwijl [6]-radialenen meestal een stoelconformatie vertonen; er zijn echter ook [6]-radialenen met een vlakke conformatie bekend.[7]
Dankzij hun bijzondere schikking van π-elektronen zijn radialenen onderzocht als potentiële bouwstenen van organische geleiders of organische ferromagneten.
Zie ook
Bronnen, noten en/of referenties
|