Natriumoxalaat
Natriumoxalaat (Na2C2O4) is een hygroscopisch natriumzout van oxaalzuur. De stof komt voor als kleurloze kristallen of als een wit poeder, en is matig oplosbaar in water. Natriumoxalaat kan optreden als reductor in chemische syntheses.
Natriumoxalaat
| ||||
| Structuurformule en molecuulmodel | ||||
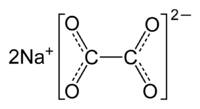 | ||||
Structuurformule van natriumoxalaat | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | Na2C2O4 | |||
| IUPAC-naam | natriumethaandioaat | |||
| Andere namen | natriumoxalaat | |||
| Molmassa | 133,9985386 g/mol | |||
| CAS-nummer | 62-76-0 | |||
| EG-nummer | 200-550-3 | |||
| Beschrijving | Kleurloze kristallen of wit poeder | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H302 - H312 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P280 | |||
| Hygroscopisch? | ja | |||
| Opslag | Gescheiden van sterk oxiderende stoffen, voeding en voedingsmiddelen. | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos of wit | |||
| Dichtheid | 2,34 g/cm³ | |||
| Smeltpunt | 250-270 °C | |||
| Goed oplosbaar in | water | |||
| Onoplosbaar in | ethanol, di-ethylether | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Natriumoxalaat kan op 2 manieren worden bereid:
- Door de zuur-basereactie van oxaalzuur met natriumhydroxide:
- Door een thermolyse van natriumformiaat bij 360°C:
Externe links
This article is issued from
Wikipedia.
The text is licensed under Creative
Commons - Attribution - Sharealike.
Additional terms may apply for the media files.
