Natriumhydride
Natriumhydride is een zout bestaande uit een natrium- en een hydride-ion. Het wordt in de organische chemie onder andere gebruikt om de geconjugeerde base van een molecuul te vormen. Bij contact met water kan natriumhydroxide en waterstof gevormd worden.
Natriumhydride
| ||||
| Structuurformule en molecuulmodel | ||||
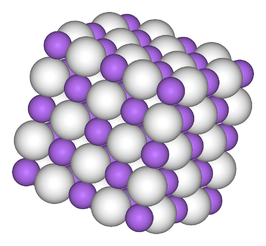 | ||||
Structuur van natriumhydride | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | NaH | |||
| Molmassa | 23,99 g/mol | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Dichtheid | 1,396 g/cm³ | |||
| Smeltpunt | 800 °C | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Wanneer natriumhydride wordt opgelost in een geschikt oplosmiddel, dissocieert het in een Na+ ion en een H− ion. Binnen de organische chemie wordt natriumhydride gebruikt als sterke base. Het wordt gebruikt als vervanger van natriumamide gezien de lagere reactiviteit met water. Het wordt gebruikt voor het deprotoneren van verschillende organische verbindingen. Het wordt echter vaak vervangen door minder nucleofiele basen, als lithiumdiisopropylamide en Lithiumbis(trimethylsilyl)amide.
Geplaatst op: 29-04-2007 |
Dit artikel is een beginnetje over scheikunde. U wordt uitgenodigd om op bewerken te klikken om uw kennis aan dit artikel toe te voegen. |
This article is issued from
Wikipedia.
The text is licensed under Creative
Commons - Attribution - Sharealike.
Additional terms may apply for the media files.