Ethylacetoacetaat
Ethylacetoacetaat of EAA is een organische verbinding met als brutoformule C6H10O3. De stof komt voor als een kleurloze, licht-viskeuze vloeistof met een kenmerkende citrusachtige geur, die matig oplosbaar is in water.
Ethylacetoacetaat
| ||||
| Structuurformule en molecuulmodel | ||||
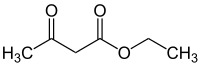 | ||||
Structuurformule van ethylacetoacetaat | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | C6H10O3 | |||
| IUPAC-naam | ethyl-3-oxobutanoaat | |||
| Andere namen | EAA, acetoazijnzure ethylester, acetylazijnzure ethylester, 3-oxobutaanzure ethylester, 1-ethoxybutaan-1,3-dion | |||
| Molmassa | 130,1418 g/mol | |||
| SMILES | CC(=O)CC(=O)OCC | |||
| CAS-nummer | 141-97-9 | |||
| Beschrijving | Kleurloze vloeistof | |||
| Vergelijkbaar met | methylacetoacetaat | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H319 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P305+P351+P338 | |||
| Opslag | Gescheiden van oxiderende stoffen. | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,021 g/cm³ | |||
| Smeltpunt | −44 °C | |||
| Kookpunt | 180,8 °C | |||
| Vlampunt | (gesloten vat) 70 °C | |||
| Zelfontbrandings- temperatuur | 295 °C | |||
| Dampdruk | 100 Pa | |||
| Oplosbaarheid in water | 125 g/l | |||
| Goed oplosbaar in | water, organische oplosmiddelen | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Synthese
Ethylacetoacetaat wordt bereid uit een reactie van ethanol en diketeen via een nucleofiel reactiemechanisme:
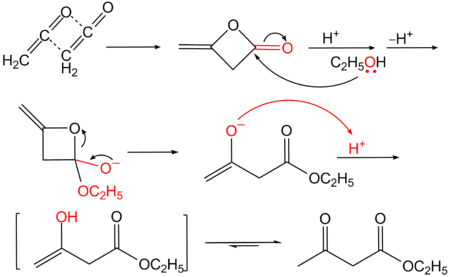 Synthese van ethylacetoacetaat uit diketeen.
Synthese van ethylacetoacetaat uit diketeen.
Het nucleofiel vrij elektronenpaar van de hydroxylgroep in ethanol valt aan op de carbonylgroep in diketeen, waarbij een alkoxide ontstaat. De carbonylgroep hervormt zich, waardoor een ringopening plaatsgrijpt en een enolaat ontstaat. Dit enolaat wordt geprotoneerd tot het enol, dat tautomeriseert tot de stabielere keto-vorm.
Een alternatieve bereidingswijze is een Claisen-condensatie van ethylacetaat. Deze methode werd voor het eerst toegepast door de Duitse scheikundige Johannes Wislicenus. Hierbij wordt 75% ethylacetoacetaat gevormd, de rest is ethanol:
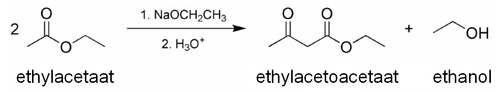 Synthese van ethylacetoacetaat uit ethylacetaat.
Synthese van ethylacetoacetaat uit ethylacetaat.
Toepassingen
Ethylacetoacetaat wordt vaak gebruikt bij de synthese van acetoacetaat-esters. Verdere wordt het gebruikt als oplosmiddel bij onder andere organische syntheses.
Toxicologie en veiligheid
Ethylacetoacetaat reageert met sterk oxiderende stoffen, waardoor brand- of ontploffingsgevaar ontstaat.
De stof is irriterend voor de ogen, de huid en de luchtwegen.
Externe links

- (en) INCHEM-sheet van ethylacetoacetaat
- (en) Gegevens van Ethylacetoacetaat in de GESTIS-stoffendatabank van het Duitse Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA) (JavaScript vereist)
