Bariumperoxide
Bariumperoxide (BaO2) is het peroxide van barium. De stof komt voor als een wit tot grijswit poeder, dat slecht oplosbaar is in water. Het is een van de meest voorkomende anorganische peroxides.
Bariumperoxide
| ||||
| Structuurformule en molecuulmodel | ||||
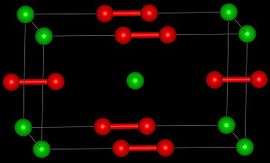 | ||||
Roosterstructuur van bariumchloride | ||||
Bariumperoxidepoeder | ||||
| Algemeen | ||||
| Molecuulformule (uitleg) | BaO2 | |||
| IUPAC-naam | bariumperoxide | |||
| Molmassa | 169,3388 g/mol | |||
| CAS-nummer | 1304-29-6 | |||
| EG-nummer | 215-128-4 | |||
| Beschrijving | Wit tot grijswit poeder | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H272 - H302 - H332 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P220 | |||
| Opslag | Gescheiden van brandbare en reducerende stoffen, voeding en voedingsmiddelen. Droog opslaan. | |||
| EG-Index-nummer | 056-001-00-1 | |||
| VN-nummer | 1449 | |||
| ADR-klasse | Gevarenklasse 5.1 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit-grijswit | |||
| Dichtheid | 5,68 g/cm³ | |||
| Smeltpunt | 450 °C | |||
| Kookpunt | 800 °C | |||
| Slecht oplosbaar in | water | |||
| Geometrie en kristalstructuur | ||||
| Kristalstructuur | tetragonaal | |||
| Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Toepassingen
Aangezien het een sterke oxidator is, wordt het onder andere gebruikt voor het bleken. Bariumperoxide wordt ook gebruikt in de pyrotechniek en vuurwerk als kleurstof: dit zout geeft een helder groene kleur.
Vroeger speelde bariumperoxide een belangrijke rol bij de bereiding van waterstofperoxide volgens onderstaand driestapsproces:
Toxicologie en veiligheid
De stof ontleedt bij verhitting en bij contact met water of zuren, met vorming van zuurstof en waterstofperoxide, die het brandgevaar verhogen. De stof is een sterk oxidatiemiddel en reageert hevig met brandbare en reducerende stoffen.
De stof is irriterend voor de ogen, de huid en de luchtwegen. De stof kan, bij blootstelling, effecten hebben op het zenuwstelsel en ze zou ook hypokalemie kunnen veroorzaken, met als gevolg hartritmestoornissen en spierstoornissen. Herhaaldelijke of langdurige blootstelling kan de dood veroorzaken.
Externe links

- (en) Gegevens van Bariumperoxide in de GESTIS-stoffendatabank van het Duitse Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA) (JavaScript vereist)
- (en) MSDS van bariumperoxide

