Empty nose syndrome
In de keel- neus- en oorheelkunde beschrijft empty nose syndrome (ENS) een neus die fysiologisch is verminkt door overmatige chirurgische verwijdering van neusschelpen (vooral de onderste neusschelpen) in een chirurgische procedure die bekendstaat als “conchareductie" of “conchotomie”. Het is daarom een iatrogene aandoening.
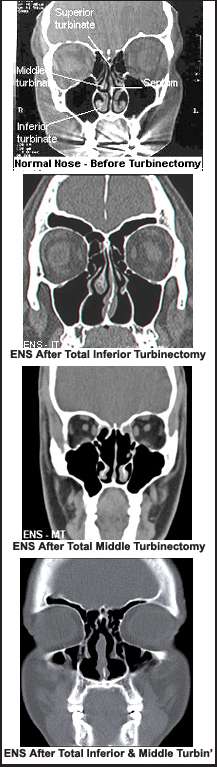
Belangrijkste symptomen
De twee belangrijkste lichamelijke symptomen zijn:
- Chronisch droge neus – Leidt vaak tot chronische slijmvliesontsteking en pijn. Chronische ontsteking kan ertoe leiden dat gebieden van het slijmvlies atrofisch worden en dit is de reden waarom sommige studies naar deze toestand verwijzen als "secundaire atrofische rinitis".[1][2][3][4][5] Minstens één grote studie concludeerde dat het gemiddeld 7,1 jaar kan duren voordat symptomen van atrofische rinitis verschijnen en dringt er bij de onderzoekende arts op aan te zoeken naar vroege tekenen en te proberen om ze tegen te gaan met zelf toegediende dagelijkse neusspoelingen en bevochtiging door de patiënt.[6]
- Paradoxale obstructie – Het gevoel dat de neus verstopt is, vaak samengaand met een constant of dikwijls optredend verontrustend gevoel van verstikking of benauwdheid, dat wordt veroorzaakt door een slechte terugkoppeling van luchtstroomsensatie door het neusslijmvlies, hetzij als gevolg van atrofie van de zenuwuiteinden van de nervus trigeminus die wordt verondersteld deze sensatie op te wekken, hun gebrek aan reactievermogen doordat het slijmvlies te droog wordt of metaplasie ondergaat, of gewoon vanwege het verlies van de normale aerodynamica van de neus na de conchareductie. Zonder een goede en constante luchtstroomsensatie van lucht die door de neus stroomt, is het terugkoppelsignaal dat de zenuwen aan het centraal zenuwstelsel geven het gevoel van benauwdheid of zijn er ongedifferentieerde ademhalingsmoeilijkheden.[7][8][9]
Andere overheersende symptomen zijn gebrek aan goede nachtrust en chronische vermoeidheid.[10] De chronische aard van de lichamelijke symptomen heeft een belangrijke invloed op de levenskwaliteit en het welzijn van de patiënt, en veroorzaakt moeite met concentreren, bezorgdheid over symptomen, angst en klinische depressie.[11] Ook de ontwikkeling van astma en chronische bronchitis is niet ongewoon, aangezien de neus de beschermer van de longen is.[12][13][14]
Ontstaanswijze
Het is bekend dat de neusschelpen de belangrijkste structuren van de neus zijn die lucht bevochtigen, warmte uitwisselen, lucht filteren, luchtstroom sturen en luchtstroom voelen. Ze sturen, verwarmen, bevochtigen en filteren de luchtstroom door deze rondom zich heen te stroomlijnen terwijl de lucht door de neus beweegt, waardoor het slijmvliesoppervlak dat in contact komt met de luchtstroom aanzienlijk wordt vergroot. Hun volledigheid en functie is van cruciaal belang voor het behoud van de gezondheid en fysiologie van neus en bijholten. Ze zijn aerodynamisch van bouw van voor naar achter en ontworpen om de ademhaling niet te veel te belemmeren terwijl ze de luchtstroom bewerken.[15]
De neusschelpen spelen een essentiële rol in de bescherming van de binnenste neusslijmvliezen en in het laten herstellen en regenereren ervan. Een normale neus van een volwassene bewerkt gemiddeld 10.000 liter lucht per 24 uur, en heeft dan ook een rustperiode nodig om te herstellen en een goede gezondheid en integriteit te behouden van de laag van delicaat luchtwegepitheel dat de nasale luchtweg en bijholten geheel bekleedt. Het herstel van de neus komt tot stand door een fenomeen dat de neuscyclus heet. Elke 3-6 uur zwelt één kant van de neus op met bloed terwijl de andere kant minder gezwollen blijft. Zo wordt het grootste deel van de werklast van de ademhaling gedragen door de niet gezwollen kant, terwijl de opgezwollen kant rust en herstelt. Als een onderste neusschelp verkleind of weggesneden is, kan de neuscyclus de kant waar dat is gebeurd niet meer volledig laten opzwellen, en is dus veel van het natuurlijke herstelvermogen van die kant verloren gegaan.[16]
Er zijn meestal drie paar neusschelpen in de menselijke neus: de onderste, de middelste en de bovenste neusschelpen. Elk paar is verschillend van afmeting en vorm, en elk beschermt een ander gebied van de neusholte. De onderste neusschelpen zijn de grootste en strekken zich uit over het gehele onderste deel van de neusholte, vanaf de voorzijde van de neus tot bijna de neuskeelholte. Aangezien de onderste neusschelpen de grootste zijn en de eerste die de ingeademde lucht verzachten, heeft hun verlies het meest radicale effect op de fysiologie van het resterende slijmvlies. De middelste neusschelpen zweven boven de onderste neusschelpen en beginnen vanaf ongeveer het middendeel van de neusholte. Zij zijn veel kleiner en herbergen, in tegenstelling tot de onderste neusschelpen, enkele uiteinden van reukzenuw en beschermen het bovenste deel van de neusholte, in het bijzonder de bundel reukzenuwen in het dak van de neus en de openingen van de zeefbeen- en voorhoofdsholten. Verlies ervan zal een kleinere rol spelen in de algehele vermindering van de in de neus vastgehouden warmte en vochtigheid, maar het kan de kwaliteit van de reukzin en de gezondheid van de zeefbeen- en voorhoofdsholten beïnvloeden. De bovenste neusschelpen zijn zeer klein in vergelijking met de onderste en middelste en hebben als enige rol de laatste beschermingslinie te zijn rond de bulbus olfactorius.
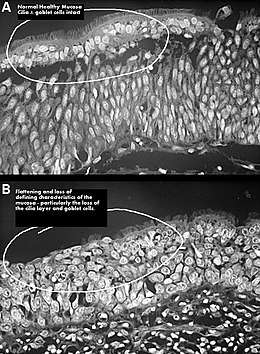
Het verlies van te veel neusschelpweefsel kan tot gevolg hebben dat het resterende slijmvlies in de nabijheid van de plaats van verwijdering en direct achter en boven dat gebied geleidelijk steeds meer ontstoken raakt, droger wordt, metaplasie en endertitis ondergaat en uiteindelijk atrofisch wordt. Als gevolg hiervan worden alle vier de functies van de neus aangetast: ademhaling, verdediging, reukzin en klankvorming. Het kan vele jaren duren voordat deze aantasting volledig tot ontwikkeling komt, hetgeen de juiste diagnose bemoeilijkt. ENS wordt soms gezien bij patiënten die relatief weinig neusschelpweefsel verloren hebben en wier neusschelpen een bijna normale omvang lijken te hebben.[10] Dit geldt in het bijzonder wanneer het voorste deel van de onderste neusschelp is weggesneden, gezien de belangrijke rol die dit deel speelt in de inwendige neusklep.[10] ENS symptomen worden door patiënten vaak snel na een conchareductie gevoeld.[10]
Diagnose
ENS kan gediagnosticeerd worden wanneer de volgende bevindingen aanwezig zijn: de patiënt klaagt over een slechte neusademhaling en vaak een meedogenloos gevoel van verstikking of kortademigheid, ondanks dat de nasale luchtweg duidelijk (meestal overduidelijk) open is. De patiënten klagen meestal ook over droogheid in de neus. Deze symptomen verschenen pas nadat de patiënt een conchareductie ondergaan had, soms vele jaren later.
Bij onderzoek zou de neusholte er abnormaal ruim uit moeten zien door het ontbreken van (een deel van) de onderste en/of middelste neusschelpen. Slijmvliespathologie varieert sterk. Bij sommige patiënten is het slijmvlies droog en bleek als gevolg van metaplasie, in andere is het rood als gevolg van chronische ontsteking. Korstvorming kan variëren van afwezig tot ernstig. De symptomen en bevindingen worden verondersteld te worden veroorzaakt door abnormale aerodynamica, chronische ontstekingen en droogte, die leiden tot het verlies van het voelen van luchtstroom, hetgeen voelt als benauwdheid.[17]
De diagnose is vaak moeilijk omdat de resterende weefsels (in reactie op de droogte en constante verergering door overturbulente luchtstromen) gewoonlijk hypertrofisch blijken te zijn.
Prognose
Er is zeer weinig onderzoek gedaan naar deze aandoening en nauwelijks langetermijnfollow-ups. Al vele jaren werd deze aandoening over het hoofd gezien of verkeerd geïnterpreteerd vanwege secundaire problemen die meestal optreden na radicale conchareducties. Bijvoorbeeld, de resterende slijmvliesstructuren (het neustussenschot en de resterende neusschelpen) worden vaak hypertrofisch, waardoor er een werkelijke fysieke obstructie ontstaat boven op de reeds bestaande paradoxale obstructie.
Het ontbreken van langetermijnfollow-up van patiënten met deze aandoening maakt het moeilijk om het percentage patiënten te schatten, dat eventueel een spontane genezing of althans een voldoende grote verbetering van hun symptomen verkrijgt. Maar, gezien het feit dat het verlies van de normale inwendige neusanatomie de belangrijkste oorzaak van de symptomen is, is het niet waarschijnlijk dat deze aandoening uit zichzelf kan genezen.
Dr. Eugene Kern, die de term "empty nose syndrome ' bedacht, beweert dat deze aandoening vaak erger wordt door de jaren heen door toenemende slijtage van het resterende slijmvlies in de neusholte, omdat het gebrek aan neusschelpen het slijmvlies blootstelt aan bovenmatig grote stromingen van ongefilterde en onbewerkte lucht bij elke inademing. Sterker nog, hij beweert dat er een onbekende drempel in verlies van neusschelpweefsel is, waarboven het neusslijmvlies zich niet kan herstellen van de dagelijkse aanval van de directe luchtstroom. Kern en Moore voerden een grote retrospectieve studie uit met 242 patiënten die zij tussen 1982 en 1999 zorgvuldig onderzochten in de Mayo Clinic in Rochester (MN, USA), en die allen een vorm van gedeeltelijke of radicale conchareductie hadden ondergaan, waarna ze symptomen van atrofische rinitis kregen. Ze noemden deze aandoening “empty nose syndrome” (legeneussyndroom) om duidelijk te maken hoe onnatuurlijk deze neuzen eruitzagen in CT-onderzoek en bij lichamelijk onderzoek. Ze benadrukten hoe zeer deze aandoening de levenskwaliteit en het welzijn van de patiënten had aangetast en het feit dat bij veel van de patiënten de symptomen door de jaren heen leken te verergeren, wijzend op verdere schade en slijtage als gevolg van het verlies van bescherming door neusschelpen, omdat er geen andere oorzaak was die dit zou kunnen verklaren.[6]
Hun bevindingen bevestigden vroege conclusies over conchareductie die werden aangenomen door kno-gemeenschappen wereldwijd nadat deze operaties aan het eind van de 19e eeuw waren gestart, en die bovendien worden onderbouwd door verschillende prominente andere studies uit het eind van de 20e eeuw die patiënten bestudeerden die radicale onderste neusschelpverwijdering hadden ondergaan. Desalniettemin zijn sommige aanhangers van conchareducties nog niet overtuigd, aangezien er een aantal langetermijnfollow-upstudies zijn die beweren geen grote ongewenste langetermijneffecten te hebben gevonden. De controverse blijft daardoor bestaan, hoewel bij de meeste neuschirurgen de slinger tegenwoordig is teruggezwenkt in de richting van het belang van het behoud van zo veel mogelijk neusschelpweefsel bij het uitvoeren van conchareducties.[18]
Om de risico's van slijmvliesatrofie te verminderen kunnen patiënten iets van het verloren vocht vervangen door hun inwendige neusoppervlak te bestrijken met beschermende gels en het gebruik van zoutenevelsprays en spoelingen, maar het lijkt erop dat, tenzij de neusschelpen functioneel worden gereconstrueerd, er weinig hoop is op volledig herstel van deze aandoening.
Er zijn er verscheidene rapportages geweest over pogingen de onderste neusschelpen te reconstrueren door implantatie van verschillende implantatiematerialen onder het slijmvlies, in een poging de normale nasale aerodynamica en fysiologie herstellen. Het aantal patiënten over wie werd gerapporteerd, was erg klein en de follow-up was relatief kort, maar de resultaten gaven enige hoop.[10][19][20] Een studie die in 2010 werd gepubliceerd, concludeerde dat operatieve verkleining van de open dwarsdoorsnede van een ‘empty nose’ om de aerodynamica positief te beïnvloeden en om de weerstand in de luchtweg te vergroten evenwel niet de luchtbewerkende functie van de neus verandert, die dus onherstelbaar beschadigd is.[9] Een andere studie rapporteerde dat, wanneer trilhaarcellen verloren zijn gegaan door degeneratie van het neusslijmvlies, zelfs operatieve sluiting van de neusgaten het aantal trilharen niet meer doet toenemen.[6]
Er is hoop bij patiënten dat met de vooruitgang in regeneratieve geneeskunde kno-artsen naar manieren zullen gaan zoeken om stamcel- en weefselmanipulatietechnologie te gebruiken om de onderste neusschelpen volledig te reconstrueren.
Momenteel beschikbare behandelingsopties
Niet-chirurgische behandeling
Niet-chirurgische behandelingsopties zijn bedoeld om de gezondheid van het resterende neusslijmvlies in de ENS-neus te behouden en te verbeteren door dit vochtig en vrij van infecties en irritatie te houden en door het in stand houden van een goede bloedtoevoer:
- De neuspassages vochtig houden met sprays of gels op basis van een zoutoplossing.
- Neusspoelingen met een gewone zoutoplossing (Veel patiënten geven de voorkeur aan het gebruik van ringerlactaatoplossing met toegevoegd xylitol, omdat ze vinden dat dit het slijmvlies meer verzacht dan gewone zoutoplossing, en er zijn een aantal empirische studies die deze bewering bevestigen).
- Spoelingen met zoutoplossing met 80 mg gentamycine als ozaena optreedt.
- Systemische medicijnen zoals geïndiceerd voor pijn en of depressie welke vaak optreedt (ongeveer 50%) bij patiënten met dit syndroom.
- Slapen met een koelemistluchtbevochtiger.
- Gewone dagelijkse lichaamsbeweging en behoud van een goede algemene gezondheid om het risico van verslechtering van de symptomen te verminderen.
Chirurgische behandeling
Chirurgische behandeling omvat het weer vernauwen van de te veel vergrote neusholte, hetzij door het verdikken van de gedeeltelijk weggesneden neusschelpen met biologisch implantatiemateriaal (wanneer ten minste 50% van de onderste neusschelpen overgebleven zijn van anterior naar posterior), hetzij door kunstmatige neusschelpen te maken door submucosale implantatie tussen submucosa en bot op belangrijke plaatsen in de neusholte. In sommige gevallen een gecombineerde aanpak de beste keuze. Het grootste probleem met implantatiechirurgie is het behalen van een duurzame volumevergroting die niet wordt geabsorbeerd met de tijd. Soms moet een procedure meerdere keren worden herhaald om een duurzaam resultaat te verkrijgen. De fysiologische locatie voor een implantaat is de zijwand van de neusholte, vanwaar de onderste neusschelpen oorspronkelijk uitstaken. Een eenvoudigere locatie voor implantatie is het neustussenschot, maar deze is minder gunstig omdat het niet de natuurlijke ligging van de neusschelpen is en het de luchtstroom te veel kan belemmeren.
De achterliggende gedachte van de operatie is de natuurlijke geometrie van de contouren van de luchtpassages in de neus (de onderste, middelste en bovenste neusgangen) zo veel mogelijk te herstellen, om de luchtstroom net genoeg te verminderen om de normale waarden van inwendige neusvochtigheid en -temperatuur terug te krijgen, waardoor het slijmvlies zich kan herstellen en de luchtstroom goed genoeg gevoeld wordt. Het is van belang om dit te doen terwijl men probeert de normale aerodynamica van de luchtstroom in de neus te herstellen, anders zal neusverstopping optreden.
Prechirurgische planning heeft impact op het succes van de procedure. De chirurg wordt geadviseerd om voorafgaand aan de implantatie een wattentest uit te voeren: de chirurg plaatst in zoutoplossing gedrenkte stukjes watten op de vooraf geplande plaats van implantatie om het implantaat te simuleren. Hierdoor beperkt en normaliseert hij de nasale luchtstromingspatronen. Dit herstelt iets van de nasale aerodynamica. Door verschillende locaties uit te proberen overeenkomstig de feedback van de patiënt over de kwaliteit van de ademhaling en andere ENS-symptomen is het mogelijk om de exacte positie van de implantaten en hun geschatte vorm en grootte vast te stellen.
Neusschelpweefsel is uniek en er zijn geen potentiële donorplaatsen in het lichaam waaruit gelijkaardig weefsel is te oogsten. In de neus is vorm echter gelijk aan functie. Het is dus mogelijk om enige functie te herstellen door herstel van de natuurlijke contouren en verhoudingen van de neuspassages: Het is mogelijk om in de neusholten een kunstmatige structuur te maken die lijkt op een neusschelp, en om zo weer iets terug te winnen van de capaciteit van de neus om de luchtstroom adequaat te weerstaan, stroomlijnen, verwarmen, bevochtigen, filteren en voelen.[10]
Implantatiematerialen
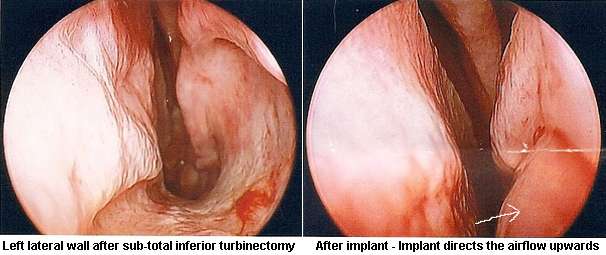
Het verdikken van submucosa en mucosa om een kunstmatige neusschelp te creëren, kan bereikt worden door het implanteren van enig ondersteunend materiaal tussen het bot / kraakbeen en ook in de submucosale laag. Veel materialen zijn geprobeerd. In de meeste gevallen werd de operatie verricht om warmte en vochtigheid terug te brengen in atrofische neuzen.
In het algemeen kunnen de implantatiematerialen worden verdeeld in 3 groepen:
- Autograften: bot, kraakbeen, vet, enzovoort van de ene plaats naar de andere bij dezelfde patiënt. De problemen zijn een relatief tekort aan weefsel en langetermijnstudies hebben hoge absorptiesnelheden in de neus aangetoond. Een Chinese studie rapporteerde succes op lange termijn met behulp van autograften van iliacaal bot.[21]
- Vreemde materialen: zoals fibrine lijm, Teflon, Gore-Tex, en plastipore, die het probleem van tekort aan autograften oplossen, gemakkelijk te vormen zijn en niet de neiging hebben om geabsorbeerd te worden. Maar ze hebben een hoge uitdrijvingsgraad, en veroorzaken soms een infectie. Een case study van een goede retentie van hydroxyapatiet cement bij één patiënt is in 2000 gemeld, maar de follow-up was slechts 1 jaar lang.[22]
- Allograften: In de laatste twee decennia zijn wetenschappers in staat geweest om een aantal basale menselijke weefsels (zoals huid) van donoren te oogsten en er genetische markers uit te verwijderen, en daarmee een menselijk natuurlijk implantatiemateriaal te leveren dat het immuunsysteem niet stimuleert het te verwerpen. Een goed voorbeeld van zo'n materiaal is acellulaire huid (merknaam "AlloDerm"). Het wordt niet afgestoten en behoudt in de meeste gebieden het grootste deel van het volume gedurende lange perioden.[10]
Het ideale implantatiemateriaal, anders dan echt origineel neusschelpweefsel, moet iets zijn met lage uitdrijvings- en afstotingsgraden, minimaal infectierisico, en een structuur bieden die sterk en verdraaglijk genoeg is en tegelijkertijd goede doorlaatbaarheid biedt voor bloedvatinlijving, wat de sleutel lijkt te zijn tegen langetermijnabsorptie.
Extra afbeeldingen
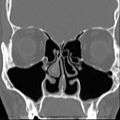 Empty Nose Syndrome na subtotale onderste conchotomie.
Empty Nose Syndrome na subtotale onderste conchotomie.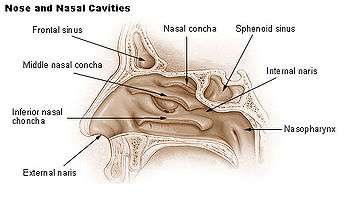 Alle neusschelpen verwijderd – Aanblik van rechter laterale wand.
Alle neusschelpen verwijderd – Aanblik van rechter laterale wand.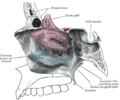 Anatomie van de neusholte
Anatomie van de neusholte
Externe links
- Empty Nose Syndrome Association (meer symptomen en een “Turbinates Tutorial” over levensbedreigende risico's in ENS)
- Dr Houser's zelfstudiepagina's over ENS
- Forum voor ENS-patiënten
- "Sniffing At Empty Nose Idea" (Aaron Zitner, The Los Angeles Times, 2001)
Referenties
- Cottle MH. Nasal Atrophy, Atrophic Rhinitis, Ozena: Medical and Surgical Treatment. Journal Of The International College Of Surgeons. Volume 29(4), pages 472-484, 1958.
- Passàli D, Lauriello M, Anselmi M, et al. Treatment of the inferior turbinate: long-term results of 382 patients randomly assigned to therapy. Ann Otol Rhinol Laryngol. 1999;108:569-75.
- Moore GF, Freeman TJ, Yonkers AJ, Ogren FP. Extended follow-up of total inferior turbinate resection for relief of chronic nasal obstruction. by in Laryngoscope, volume 95, September 1985.
- Berenholz L, et al'. Chronic Sinusitis: A sequela of Inferior Turbinectomy. American Journal of Rhinology, July–August 1998, volume 12, number 4.
- Wang Y, Liu T, Qu Y, Dong Z, Yang Z. Empty nose syndrome. Zhonghua Er Bi Yan Hou Ke Za Zhi. 2001 Jun;36(3):203-5.
- Moore EJ & Kern EB. Atrophic rhinitis: A review of 242 cases. American Journal of Rhinology, 15(6), 2001.
- Clarke RW, Jones AS, Charters P, et al. The role of mucosal receptors in the nasal sensation of airflow. Clin Otolaryngol. 1992;17:383-87.
- Chhabra N. and Houser SM. The diagnosis and management of empty nose syndrome. Otolaryngologic Clinics of north America. 2009 (April);42(2):311-330,ix.
- Scheithauer MO. Surgery of the turbinates and “empty nose” syndrome. GMS Current Topics in Otorhinolaryngology – Head and Neck Surgery 2010. Vol 9:Doc03. doi: 10.3205/cto000067
- Houser SM. Surgical Treatment for Empty Nose Syndrome. Archives of Otolaryngology Head & Neck Surgery\ Vol 133 (No.9) Sep' 2007: 858-863.
- Rice DH, Kern EB, Marple BF, Mabry RL, Friedman WH. The turbinates in nasal and sinus surgery: a consensus statement. Ear Nose Throat J. 2003;82(2):82-84.
- Bionity Life Science Encyclopedia on empty nose syndrome.
- Hens G, Hellings PW. The nose: gatekeeper and trigger of bronchial disease, Rhinology 2006 Sep; 44(3):179-87.
- Hellings PW, Prokopakis EP. Global airway disease beyond allergy, Curr Allergy Asthma Rep. 2010 Mar;10(2):143-9.
- Wolf M, Naftali S, Schroter RC, Elad D. Air-conditioning characteristics of the human nose. The Journal of Laryngology & Otology February 2004, Vol. 118, pp. 87–92.
- Hasegawa M, Kern EB. The human nasal cycle. Mayo Clin Proc. 1977 Jan;52(1):28-34.
- Huizing & de-Groot, Functional Reconstructive Nasal Surgery. Thieme (2003), p. 64–65. ISBN 1-58890-081-9.
- Hol MKS. & Huizing EH. Treatment of inferior turbinate pathology: a review and critical evaluation of the different techniques. Rhinology, 38, 157-166, 2000.
- Wang Y, Liu T, Qu Y, Dong Z, Yang Z. Empty Nose Synrome. Zhonghua Er Bi Yan Hou Ke Za Zhi. 2001 Jun;36(3):203-5. Chinese.
- Rice DH. Rebuilding the inferior turbinate with hydroxyapatite cement. Ear Nose Throat J. 2000 Apr;79(4):276-7.
- Wang Y, Liu T, Qu Y, et al. [Empty nose syndrome]. Zhonghua Er Bi Yan Hou Ke Za Zhi 2001;36(3):203–5 [Chinees].
- Rice DH. Rebuilding the inferior turbinate with hydroxyapatite cement. Ear Nose Throat J 2000;79(4):276–7.